题目内容
9.铜片、锌片连接后浸入稀硫酸中构成原电池,当导线上通过3.01×1022个电子时,锌失去电子0.05mol,铜片表面析出氢气0.56L(标准状况).分析 锌比铜活泼,形成原电池反应时,锌为负极,发生氧化反应,电极反应式为Zn-2e-=Zn2+,铜为正极,发生还原反应,电极反应式为2H++2e-=H2↑,结合电极反应式进行相关的计算.
解答 解:锌比铜活泼,形成原电池反应时,锌为负极,发生氧化反应,电极反应式为Zn-2e-=Zn2+,铜为正极,发生还原反应,电极反应式为2H++2e-=H2↑,
当导线上通过3.01×1022个电子时,转移电子为$\frac{3.01×1{0}^{22}}{6.02×1{0}^{23}/mol}$=0.05mol,铜片表面析出氢气体积为0.025mol×22.4L/mol=0.56L,
故答案为:0.05;0.56.
点评 本题考查原电池知识,为高考常见题型,侧重于学生的分析能力和计算能力的考查,注意把握电极反应式的书写,题目难度不大.

练习册系列答案
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
3.Na2FeO4是一种高效多功能水处理剂,既能消毒杀菌,又能除去悬浮物杂质.一种制备Na2FeO4的方法为2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑,下列有关说法正确的是( )
| A. | 在反应中氧化剂是Na2O2,还原剂是FeSO4 | |
| B. | 生成2molNa2FeO4时,反应中共有8mol电子转移 | |
| C. | 反应中生成22.4LO2时,共有10mol电子转移 | |
| D. | Na2FeO4净水过程中,既有氧化还原反应发生,又有非氧化还原反应发生 |
17.设NA为阿伏加德罗常数的值.下列说法正确的是(O-16Fe-56)( )
| A. | 常温下,0.5 mol•L-1 Fe2(SO4)3溶液中含Fe3+数目为1 NA | |
| B. | 标准状况下,22.4L苯中含C-H数目为6NA | |
| C. | 常温常压下,16g O2和O3混合气体中,含氧原子的总数为1NA | |
| D. | 5.6g Fe与足量稀盐酸反应,转移电子数为0.3NA |
1.新能源的开发利用时人类社会可持续发展的重要课题.下列属于新能源的是( )
| A. | 煤炭 | B. | 氢气 | C. | 天然气 | D. | 石油 |
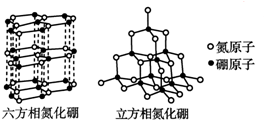 新华网合肥2011年7月21日电,安徽省矿产资源储量评审中心公布:安徽省地质矿产勘查局在本省金寨县沙坪沟探明一处世界级的巨型钼矿,钼金属总储量达到220万吨以上,潜在经济价值超过6 000亿元,钼是制备二维材料的重要金属,英国科学家因制备二维晶体材料--石墨烯获得2010年诺贝尔物理学奖,他们利用“胶带+铅笔”制得单层石墨烯(即从石墨表面剥离下来仅一个原子厚度的材料).之后,人们又制备出一些氮化硼和二硫化钼的二维晶体.根据材料提供的信息,回答相关问题.
新华网合肥2011年7月21日电,安徽省矿产资源储量评审中心公布:安徽省地质矿产勘查局在本省金寨县沙坪沟探明一处世界级的巨型钼矿,钼金属总储量达到220万吨以上,潜在经济价值超过6 000亿元,钼是制备二维材料的重要金属,英国科学家因制备二维晶体材料--石墨烯获得2010年诺贝尔物理学奖,他们利用“胶带+铅笔”制得单层石墨烯(即从石墨表面剥离下来仅一个原子厚度的材料).之后,人们又制备出一些氮化硼和二硫化钼的二维晶体.根据材料提供的信息,回答相关问题.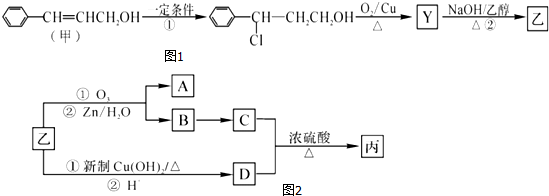
 .
. ;
;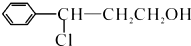 →Y:
→Y: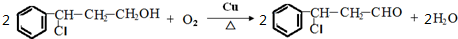 .
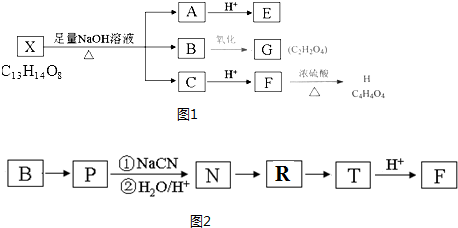
. .
.
 +(2n-1)H2O.
+(2n-1)H2O.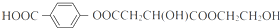 .
.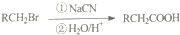
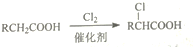

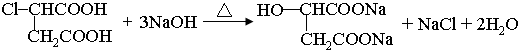 .
. ,DA4的结构式为
,DA4的结构式为 ;
;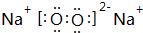 ,D元素在周期表中的位置第二周期IVA族;
,D元素在周期表中的位置第二周期IVA族;