题目内容
 俗称“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌“一滴香”的分子结构如图所示,下列说法正确的是( )
俗称“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌“一滴香”的分子结构如图所示,下列说法正确的是( )| A、该有机物的分子式为C7H6O3 |
| B、1mol该有机物最多能与2molH2发生加成反应 |
| C、该有机物能发生取代、加成和氧化反应 |
| D、该有机物的一种芳香族同分异构体能发生眼镜反应 |
考点:有机物的结构和性质
专题:
分析:由有机物的结构简式可确定有机物的分子式,该有机物中含有碳碳双键,可发生加成、加聚和氧化反应,含有C=O键,可发生加成反应,含有-OH,可发生取代、氧化反应,以此解答该题.
解答:
解:A.由有机物的结构简式可知,该有机物含有7个C原子,8个H原子和3个O原子,则分子式为C7H8O3,故A错误;
B.能与氢气发生加成反应的为C=C和C=O键,则1 mol该有机物最多能与3 mol H2发生加成反应,故B错误;
C.该有机物中含有碳碳双键,可发生加成、加聚和氧化反应,含有C=O键,可发生加成反应,含有-OH,可发生取代、氧化反应,与氢气的加成反应也为还原反应,故C正确;
D.该有机物的不饱和度为
=4,则对应的一种芳香族同分异构体中只含有苯环,不含醛基,则不能发生银镜反应,故D错误.
故选C.
B.能与氢气发生加成反应的为C=C和C=O键,则1 mol该有机物最多能与3 mol H2发生加成反应,故B错误;
C.该有机物中含有碳碳双键,可发生加成、加聚和氧化反应,含有C=O键,可发生加成反应,含有-OH,可发生取代、氧化反应,与氢气的加成反应也为还原反应,故C正确;
D.该有机物的不饱和度为
| 2×7+2-8 |
| 2 |
故选C.
点评:本题考查有机物的结构和性质,为高考常见题型和高频考点,侧重于学生的分析能力的考查,注意把握有机物的结构和官能团的性质,题目难度中等.

练习册系列答案
 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
下列判断错误的是( )
| A、沸点:NH3>PH3>AsH3 |
| B、熔点:Li>Na>K |
| C、酸性:HClO4>H2SO4>H3PO4 |
| D、碱性:NaOH>Mg(OH)2>Al(OH)3 |
乙醇分子中不同的化学键如图:关于乙醇在各种反应中断裂键的说法不正确的是( )


| A、乙醇和钠反应键②断裂 |
| B、在Ag催化下和O2反应键①③断裂 |
| C、乙醇和浓H2SO4共热,在140℃时,键①或键②断裂 |
| D、乙醇和浓H2SO4共热,在170℃时,键②⑤断裂 |
下列说法正确的是( )
A、按系统命名法, 的名称是2,3-二乙基丁烷 的名称是2,3-二乙基丁烷 |
B、某烃的衍生物A的分子式为C6H12O2,已知 ,又知D不与NaHCO3溶液反应,C和E都不能发生银镜反应,则A的结构可能有4种 ,又知D不与NaHCO3溶液反应,C和E都不能发生银镜反应,则A的结构可能有4种 |
| C、完全燃烧相同碳原子、且相同质量的烷烃、烯烃、炔烃,耗氧量最大的是烷烃 |
| D、已知烃A的分子式为C5Hm,烃B的最简式为C5Hn(m、n均为正整数),则烃A和烃B不可能互为同系物 |
根据表提供的数据,下列判断正确的是( )
| 弱酸化学式 | CH3COOH | HClO | H2CO3 |
| 电离平衡常数 | 1.8×10-5 | 3.0×10-8 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
| A、等物质的量的Na2CO3和CH3COOH两种溶液混合,一定 有:c(Na+)+c(H+)=2c(CO32-)+c (HCO3-)+c (CH3COO-) |
| B、常温下,已知酸H2A存在如下平衡:H2A?H++HA-;HA-?H++A2-(Ka1=5.9xl0-2,Ka2=6.4xl0'6),则NaHA溶液中水的电离程度一定大于纯水中水的电离程度 |
| C、相同浓度的CH3COONa和NaClO混合溶液中各离子浓度大小关系是:c (Na+)>c (ClO-)>c (CH3COO-)>c (OH-)>c (H+) |
| D、常温下,在O.lmol/LCH3COOH溶液中滴加O.lmol/LNaOH的溶液发生反应,当c(CH3COOH):c (CH3COO-)=5:9时,此时溶液pH=5 |
下列实验过程中,溶液的pH增大的是( )
| A、向NaOH溶液中滴加水 |
| B、向稀盐酸中滴加NaOH溶液 |
| C、向NaCl溶液中滴加稀盐酸 |
| D、向NaOH溶液中滴加稀盐酸 |
下列关于实验的说法正确的是( )
| A、将二氧化碳通人硅酸钠溶液以证明碳酸的酸性比硅酸强 |
B、如图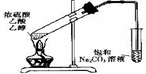 装置中,导管不能伸人液面的原因是产物易溶于水 装置中,导管不能伸人液面的原因是产物易溶于水 |
| C、用碱石灰可干燥氯气 |
| D、用普通玻璃棒蘸取溶液做焰色反应以证明溶液含有Na十 |