题目内容
已知:2CO(g)+O2(g)=2CO2(g)△H=-566kJ?mol-1
Na2O2(s)+CO2(g)═Na2CO3(s)+
O2(g)△H=-226kJ?mol-1
根据以上热化学方程式判断,下列说法正确的是( )
Na2O2(s)+CO2(g)═Na2CO3(s)+
| 1 |
| 2 |
根据以上热化学方程式判断,下列说法正确的是( )
| A、1.4g CO完全燃烧放出热量为28.3kJ |
| B、CO(g)+Na2O2(s)═Na2CO3(s)△H=-509kJ?mol-1 |
| C、2Na2O2(s)+2CO2(s)═2Na2CO3(s)+O2(g)△H<-452kJ?mol-1 |
| D、CO2(g)与Na2O2(s)反应放出226kJ热量时,电子转移为2×6.02×1023 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、据CO燃烧的热化学方程式分析;
B、利用盖斯定律解答;
C、根据热化学方程式中热量与物质的量之间的关系、物质由固态变气态吸收热量以及盖斯定律来解答;
D、据所给热化学方程式分析;
B、利用盖斯定律解答;
C、根据热化学方程式中热量与物质的量之间的关系、物质由固态变气态吸收热量以及盖斯定律来解答;
D、据所给热化学方程式分析;
解答:
解:A、据CO燃烧的热化学方程式分析可知,2.8gCO完全求算放热28.3KJ,故A错误;
B、题目中
+2式为:Na2O2(s)+CO(g)=Na2CO3(s)△H=-509 kJ/mol,故B正确;
C、题目中第二个方程的2倍为:2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g)△H=-452 kJ/mol,本题中的CO2(s)多一步变气体吸热的过程,所以本题放出的热量就少于452,但是△H>-452 kJ/mol,故C错误;
D、反应Na2O2(s)+CO2(g)═Na2CO3(s)+
O2(g)△H=-226kJ?mol-1,每有1molNa2O2(s)反应.转移1mol电子,放热226KJ,故D错误;
故选B.
B、题目中
| 1式 |
| 2 |
C、题目中第二个方程的2倍为:2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g)△H=-452 kJ/mol,本题中的CO2(s)多一步变气体吸热的过程,所以本题放出的热量就少于452,但是△H>-452 kJ/mol,故C错误;
D、反应Na2O2(s)+CO2(g)═Na2CO3(s)+
| 1 |
| 2 |
故选B.
点评:本题主要考查了燃烧热的概念、单位、盖斯定律等知识,试题的综合性较强,有一定的难度.

练习册系列答案
相关题目
在恒温、恒容的条件下,有反应2A(g)+2B(g)?C(g)+3D(g),现从两条途径分别建立平衡.途径Ⅰ:A、B的起始浓度均为2mol/L;途径Ⅱ:C、D的起始浓度分别为2mol/L和6mol/L.则以下叙述不正确的是( )
| A、两途径最终达到平衡时,体系内混合气的平均相对分子质量不同 | ||
| B、两途径最终达到平衡时,体系内混合气的百分组成相同 | ||
| C、达平衡时,途径Ⅰ的反应速率v(A)小于途径Ⅱ的反应速率v(A) | ||
D、达平衡时,途径Ⅰ所得混合气的密度为途径Ⅱ所得混合气密度的
|
下列叙述不正确的是( )
| A、把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
| B、铜锌原电池工作时,电流沿外电路从铜电极流向锌电极 |
| C、把铜片插入三氯化铁溶液中,在铜片表面出现一层铁 |
| D、为加快锌粒与盐酸反应的速率,可以向溶液中加入几滴氯化铜溶液 |
苹果汁是人们喜爱的饮料.由于饮料中含有 Fe2+离子,现榨的苹果汁在空气中会由淡绿色变为棕黄色,使Fe2+转变为Fe3+离子.若榨苹果汁时加入维生素C,可有效防止这种现象的发生.这说明维生素C具有( )
| A、氧化性 | B、还原性 |
| C、酸性 | D、碱性 |
将0.1mol Al投入3mol/L NaOH溶液100mL中,充分反应后再滴加1mol/L硫酸溶液120mL,最终结果是( )
| A、得到混浊液体 |
| B、得到澄清透明溶液 |
| C、溶液中无NaAlO2 |
| D、溶液pH=7 |
在标准状况下,进行甲、乙、丙三组实验:三组各取60mL同浓度盐酸溶液,加入同一种镁铝合金粉末,产生气体,有关数据列表如下:
则下列说法正确的是( )
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 510 | 770 | 918 |
| 气体体积/mL | 560 | 672 | 672 |
| A、甲组和乙组的实验中,盐酸均是过量的 |
| B、盐酸的物质的量浓度为0.8mol/L |
| C、合金中镁铝的物质的量之比为1:1 |
| D、丙组中铝的物质的量为0.018mol |
组成金属单质的微粒( )
| A、金属原子 |
| B、金属阳离子和电子 |
| C、金属原子和电子 |
| D、阳离子和阴离子 |
在密闭容器中发生下列反应:xA g)+y B(g)?zC(g),平衡时测得A的浓度为 0.5mol/L,保持温度不变,将容器的容积压缩到原来的
,再达平衡时测得A的浓度为 0.8mol/L,下列判断正确的是( )
| 1 |
| 2 |
| A、平衡向逆反应方向移动 |
| B、x+y>z |
| C、B的物质的量增大 |
| D、C的体积分数保持不变 |
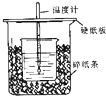 用50mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: