题目内容
11.1mol/L的CaCl2溶液0.5L,Cl-离子的物质的量浓度为2mol/L.分析 溶液中离子浓度=溶质浓度×离子数,根据c(Cl-)=2c(CaCl2)计算.
解答 解:c(Cl-)=2c(CaCl2)=2×1mol/L=2mol/L,故答案为:2.
点评 本题考查了物质的量浓度的计算,根据物质的量浓度公式结合化学式来分析解答,注意物质浓度与离子浓度的关系,题目难度不大.

练习册系列答案
相关题目
1.从某废液(含有Fe2+、Cu2+、Cl-)中回收铜并制得纯净的FeCl3溶液.现以制得纯净的FeCl3溶液为原料制取优良的水处理剂高铁酸钾(K2FeO4),其流程如图:
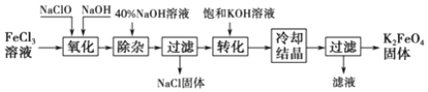
已知:高锰酸钾(K2FeO4)位暗紫色固体,可溶于水.在中性或酸性溶液中逐渐分解,在碱性溶液中稳定.高锰酸钾具有强氧化性.高锰酸钾(K2FeO4)与水作用产生Fe(OH)3.
(1)检验废液中含有Fe2+选用的试剂是KMnO4(填化学式);从废液中制得纯净的FeCl3溶液加入的试剂除铁粉外,还需要一种试剂是Cl2(填化学式),加入时发生反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-.
(2)高锰酸钾(K2FeO4)在处理水过程中的作用是杀菌消毒和净水.
(3)“氧化”过程反应的离子方程式为2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O.
(4)过滤时需用的玻璃仪器有玻璃棒、烧杯和漏斗,上述工艺得到的高锰酸钾常含有杂志,可用重结晶法提纯,操作是:将粗产品用饱和KOH溶液溶解,然后加热浓缩、冷却结晶、过滤.
(5)用回收的铜为原料可制得粗制CuSO4•5H2O晶体(含有少量的FeSO4•7H2O),除去CuSO4•5H2O晶体中杂志的方法是:向溶液中加入H2O2,再调解溶液PH,过滤即可制得纯净的CuSO4溶液,进而制得纯净CuSO4•5H2O的晶体.
已知:室温时一些物质的Kaq如表:
已知溶液中的离子浓度小于1×10-6mol•L-1时就认定沉淀完全.
加双氧水的目的是将亚铁离子氧化成铁离子;若溶液中CuSO4的浓度为3.0mol•L-1,通过计算说明此方法可除去粗制CuSO4•5H2O晶体中FeSO4•7H2O的理由通常认为溶液中的离子浓度小于1×10-6mol•L-1时就认定沉淀完全,设溶液中CuSO4的浓度为3.0mol•L-1,则Cu(OH)2开始沉淀时的PH为4,Fe3+完全沉淀时溶液的PH为3.3,通过计算确定上述方案可行.

已知:高锰酸钾(K2FeO4)位暗紫色固体,可溶于水.在中性或酸性溶液中逐渐分解,在碱性溶液中稳定.高锰酸钾具有强氧化性.高锰酸钾(K2FeO4)与水作用产生Fe(OH)3.
(1)检验废液中含有Fe2+选用的试剂是KMnO4(填化学式);从废液中制得纯净的FeCl3溶液加入的试剂除铁粉外,还需要一种试剂是Cl2(填化学式),加入时发生反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-.
(2)高锰酸钾(K2FeO4)在处理水过程中的作用是杀菌消毒和净水.
(3)“氧化”过程反应的离子方程式为2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O.
(4)过滤时需用的玻璃仪器有玻璃棒、烧杯和漏斗,上述工艺得到的高锰酸钾常含有杂志,可用重结晶法提纯,操作是:将粗产品用饱和KOH溶液溶解,然后加热浓缩、冷却结晶、过滤.
(5)用回收的铜为原料可制得粗制CuSO4•5H2O晶体(含有少量的FeSO4•7H2O),除去CuSO4•5H2O晶体中杂志的方法是:向溶液中加入H2O2,再调解溶液PH,过滤即可制得纯净的CuSO4溶液,进而制得纯净CuSO4•5H2O的晶体.
已知:室温时一些物质的Kaq如表:
| 化学式 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| Kaq | 8.0×10-16 | 8.0×10-18 | 8.0×10-20 |
加双氧水的目的是将亚铁离子氧化成铁离子;若溶液中CuSO4的浓度为3.0mol•L-1,通过计算说明此方法可除去粗制CuSO4•5H2O晶体中FeSO4•7H2O的理由通常认为溶液中的离子浓度小于1×10-6mol•L-1时就认定沉淀完全,设溶液中CuSO4的浓度为3.0mol•L-1,则Cu(OH)2开始沉淀时的PH为4,Fe3+完全沉淀时溶液的PH为3.3,通过计算确定上述方案可行.
2.容器体积不变时,对于合成氨的反应,下列状态达平衡的是( )
| A. | 氮气和氢气不再发生反应时的状态 | |
| B. | 体系中的总压强不变时的状态 | |
| C. | 氮气的浓度与氢气的浓度之比为1:3时 | |
| D. | 混合物的密度保持不变时的状态 |
19.下列各组离子中,能大量共存且加入(或通入)X试剂后发生反应的离子方程式对应正确的是( )
| 选项 | 离子组 | 试剂X | 离子方程式 |
| A | 透明溶液中:Fe3+、SO42-、NO3- | 过量的铜粉 | 2Fe3++Cu=2Fe2++Cu2+ |
| B | Cu2+、Al3+、AlO2-、Cl- | 过量的盐酸 | AlO2-+4H++=Al3++2H2O |
| C | Na+、Ba2+、HCO3-、NO3- | NaHSO4溶液 | H++HCO3--=CO2↑+H2O |
| D | pH=0的溶液中:Mg2++,Fe2++、NO3-- | 双氧水 | 2Fe2++H2O2+2H+=2Fe3++2H2O |
| A. | A | B. | B | C. | C | D. | D |
6.已知:
Na2O2(s)+CO2(g)═Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226kJ•mol-1
2CO(g)+O2(g)═2CO2(g)△H=-566kJ•mol-1
根据以上热化学方程式判断,下列说法正确的是( )
Na2O2(s)+CO2(g)═Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226kJ•mol-1
2CO(g)+O2(g)═2CO2(g)△H=-566kJ•mol-1
根据以上热化学方程式判断,下列说法正确的是( )
| A. | CO的燃烧热为283 kJ | |
| B. | 两个反应都只发生了共价键的断裂和形成 | |
| C. | CO2(g)与Na2O2(s)反应放出452kJ热量时,电子转移数为6.02×1023 | |
| D. | Na2O2(s)+CO(g)═Na2CO3(s)△H=-509 kJ/mol. |
16.下列说法正确的是( )
| A. | 能电离出H+的化合物叫做酸 | |
| B. | 摩尔是七个基本物理量之一 | |
| C. | 化合物分为酸、碱、盐和氧化物是用树状分类法分类的 | |
| D. | 实验测得1mol某气体体积为22.4L,测定条件一定是标准状况 |
3.下列操作中不正确的是( )
| A. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| B. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 过滤时,玻璃棒的末端应轻轻靠在三层滤纸处 |
1.在配制一定物质的量浓度的NaOH溶液时,下列说法正确的是( )
| A. | 将称量NaOH固体时在烧杯中溶解后立即转移到容量瓶中 | |
| B. | 向容量瓶中加水定容时俯视 所配溶液浓度偏高 | |
| C. | 配制NaOH溶液不需用到量筒 | |
| D. | 定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线 |
 .
. .
. .
. 、
、
 、
、 .
.