题目内容
将标况下一定体积的CO2气体通入1L 0.015mol/L澄清石灰水中,得到沉淀质量为1g,求通入的CO2的体积是多少?如果反应后溶液体积仍为1L,则最终溶液中Ca2+的物质的量浓度是多少?(请书写必要的计算过程)
考点:化学方程式的有关计算
专题:计算题
分析:二氧化碳通入澄清石灰水中,发生反应Ca(OH)2+CO2═CaCO3↓+H2O,CO2+CaCO3↓+H2O=Ca(HCO3)2,根据二氧化碳与氢氧化钙的量的关系计算,得到沉淀质量为1g,可能二氧化碳少量或过量,据此分析结合方程式解答.
解答:
解:少量二氧化碳通入澄清石灰水中得到沉淀Ca(OH)2+CO2═CaCO3↓+H2O,过量沉淀溶解,CO2+CaCO3↓+H2O=Ca(HCO3)2,1L 0.015mol/L澄清石灰水中n[Ca(OH)2]=cv=0.015mol/L×1L=0.015mol,得到沉淀质量为1g,n(CaCO3)=
=
=0.01mol,
当二氧化碳少量时,只发生:Ca(OH)2+CO2═CaCO3↓+H2O则:n(CO2)=n(CaCO3)=0.01mol,V=n×Vm=0.01mol×22.4mol/L=0.224L,
当二氧化碳过量时,沉淀部分溶解,先发生Ca(OH)2+CO2═CaCO3↓+H2O,则:n(CO2)=n[Ca(OH)2]=n(CaCO3)=0.015mol,再发生CO2+CaCO3↓+H2O=Ca(HCO3)2,剩余0.01mol碳酸钙,溶解0.015mol-0.01mol=0.005mol,需再铜二氧化碳0.005mol,所以需二氧化碳总共为0.015mol+0.005mol=0.02mol,V=n×Vm=0.02mol×22.4mol/L=0.448L,
1L 0.015mol/L澄清石灰水中n[Ca(OH)2]=cv=0.015mol/L×1L=0.015mol,得到沉淀质量为1g,n(CaCO3)=
=
=0.01mol,所以最终溶液中Ca2+的物质的量为0.015mol-0.01mol=0.005mol,
如果反应后溶液体积仍为1L,则最终溶液中Ca2+的物质的量浓度c=
=
=0.005mol/L,
答:二氧化碳少量时,通入的CO2的体积为0.224L,二氧化碳过量时,通入的CO2的体积为0.448L,最终溶液中Ca2+的物质的量浓度0.005mol/L;
| m |
| M |
| 1g |
| 100g/mol |
当二氧化碳少量时,只发生:Ca(OH)2+CO2═CaCO3↓+H2O则:n(CO2)=n(CaCO3)=0.01mol,V=n×Vm=0.01mol×22.4mol/L=0.224L,
当二氧化碳过量时,沉淀部分溶解,先发生Ca(OH)2+CO2═CaCO3↓+H2O,则:n(CO2)=n[Ca(OH)2]=n(CaCO3)=0.015mol,再发生CO2+CaCO3↓+H2O=Ca(HCO3)2,剩余0.01mol碳酸钙,溶解0.015mol-0.01mol=0.005mol,需再铜二氧化碳0.005mol,所以需二氧化碳总共为0.015mol+0.005mol=0.02mol,V=n×Vm=0.02mol×22.4mol/L=0.448L,
1L 0.015mol/L澄清石灰水中n[Ca(OH)2]=cv=0.015mol/L×1L=0.015mol,得到沉淀质量为1g,n(CaCO3)=
| m |
| M |
| 1g |
| 100g/mol |
如果反应后溶液体积仍为1L,则最终溶液中Ca2+的物质的量浓度c=
| n |
| v |
| 0.005mol |
| 1L |
答:二氧化碳少量时,通入的CO2的体积为0.224L,二氧化碳过量时,通入的CO2的体积为0.448L,最终溶液中Ca2+的物质的量浓度0.005mol/L;
点评:本题考查化学方程式的计算,掌握二氧化碳通入澄清石灰水中少量得到沉淀,过量沉淀溶解是解答的关键,题目难度不大.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
下列图示与对应的叙述相符的是( )
A、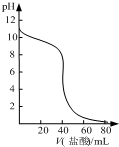 如图表示盐酸滴加到0.1mol/L某碱溶液得到的滴定曲线,用已知浓度盐酸滴定未知浓度该碱时最好选取酚酞作指示剂 |
B、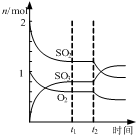 如图表示一定条件下进行的反应2SO2+O2═2SO3各成分的物质的量变化,t2时刻改变的条件可能是缩小容器体积 |
C、 如图表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20mL Ba(OH)2溶液时铝离子恰好沉淀完全 |
D、 如图表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是盐酸 |
X、Y、Z、M、W为五种短周期元素.X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15;X与Z可形成XZ2型分子;Y与M形成的气态化合物在标准状况下的密度为0.76g/L,W的质子数是X、Y、Z、M四种元素质子数之和的
.下列说法正确的是( )
| 1 |
| 2 |
| A、原子半径:W>Z>Y>X>M |
| B、XZ2、X2M2、W2Z2均为共价化合物 |
| C、由X元素形成的单质不一定能导电 |
| D、由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键 |
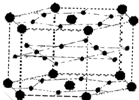 A、B、C、D、E、F六种元素,A、B、C属于第四周期且单质均为固体.基态时,A、B原子核外电子均成对,且核电荷数A>B,原子半径A<B;C与A在周期表属于同一区的元素,原子半径接近.如图是金属B和C所形成的某种合金的晶胞结构示意图;D、E、F在周期表中属于同一区,D原子在基态时p轨道半充满且电负性是同族元素中最大的;E的逐级电离能数据有两次突跃,E原子的第一电离能至第四电离能(kJ/mol)分别为:578、1817、2745、11575;F原子有三个能层,E与F能形成原子数目比为1:3,熔点为190℃的化合物Q.请回答:
A、B、C、D、E、F六种元素,A、B、C属于第四周期且单质均为固体.基态时,A、B原子核外电子均成对,且核电荷数A>B,原子半径A<B;C与A在周期表属于同一区的元素,原子半径接近.如图是金属B和C所形成的某种合金的晶胞结构示意图;D、E、F在周期表中属于同一区,D原子在基态时p轨道半充满且电负性是同族元素中最大的;E的逐级电离能数据有两次突跃,E原子的第一电离能至第四电离能(kJ/mol)分别为:578、1817、2745、11575;F原子有三个能层,E与F能形成原子数目比为1:3,熔点为190℃的化合物Q.请回答:
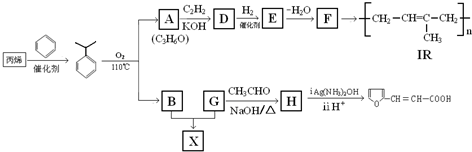
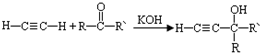
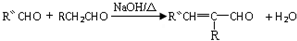 (-R、-R′、-R″表示可能相同或可能不同的原子或原子团)
(-R、-R′、-R″表示可能相同或可能不同的原子或原子团)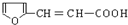 有多种同分异构体,符合下列要求的有
有多种同分异构体,符合下列要求的有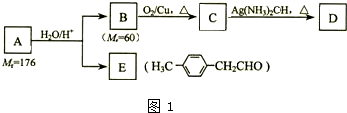 Ⅰ.已知:R-CH=CH-O-R′
Ⅰ.已知:R-CH=CH-O-R′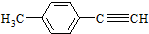 )的一条路线如图2:
)的一条路线如图2: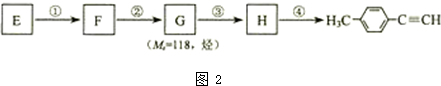
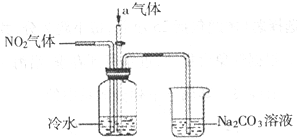
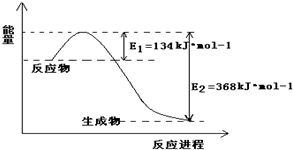 Ⅰ.(1)1molNO2和1molCO反应生成CO2和NO过程中的能量变化如图,请写出NO2和CO反应的热化学方程式
Ⅰ.(1)1molNO2和1molCO反应生成CO2和NO过程中的能量变化如图,请写出NO2和CO反应的热化学方程式