题目内容
9.在2L密闭容器中进行反应:mX(g)+nY(g)?pZ(g)+qQ(g),式中m、n、p、q为物质系数.在0min~3min 内,各物质物质的量的变化如表所示:  | X | Y | Z | Q |
| 起始(mol) | 0.7 | 1 | ||
| 2min末(mol) | 0.8 | 2.7 | 0.8 | 2.7 |
| 3min末(mol) | 0.6 |
(1)试确定以下物质的相关量:起始时n(Y)=2.3mol,n(Q)=3mol.
(2)方程式中m=1
(3)用Z表示2min内的反应速率0.05mol•L-1•min-1.
(4)2min末Q的转化率为10%.
分析 已知2min内v(Q)=0.075mol•L-1•min-1,则△n(Q)=0.075mol•L-1•min-1×2min×2=0.3mol,
根据表中数据可知,2min内X的物质的量变化为:0.8mol-0.7mol=0.1mol,
Z的物质的量变化为:1mol-0.8mol=0.2mol,
根据反应速率v(Z):v(Y)=1:2可知,Y的物质的量变化为:△n(Y)=2△n(Z)=0.4mol,
反应方程式中物质的量变化与其化学计量数成正比,则:m:n:p:q=0.1mol:0.4mol:0.2mol:0.3mol=1:4:2:3,
所以m=1、n=4、p=2、q=3,
反应的化学方程式为:X(g)+4Y(g)?2Z(g)+3Q(g),
根据以上分析进行解答.
(1)根据反应X(g)+4Y(g)?2Z(g)+3Q(g)及表中数据计算出反应初始时Y、Q的物质的量;
(2)根据以上分析可知m=1、n=4、p=2、q=3;
(3)根据反应速率的表达式v=$\frac{△c}{△t}$计算出用Z表示2min内的反应速率;
(4)根据2min内消耗的Q的物质的量及反应前Q的总物质的量计算出转化率.
解答 解:2min内v(Q)=0.075mol•L-1•min-1,则△n(Q)=0.075mol•L-1•min-1×2min×2=0.3mol,
根据表中数据可知,2min内X的物质的量变化为:0.8mol-0.7mol=0.1mol,
Z的物质的量变化为:1mol-0.8mol=0.2mol,
根据反应速率v(Z):v(Y)=1:2可知,Y的物质的量变化为:△n(Y)=2△n(Z)=0.4mol,
反应方程式中物质的量变化与其化学计量数成正比,则:m:n:p:q=0.1mol:0.4mol:0.2mol:0.3mol=1:4:2:3,
所以m=1、n=4、p=2、q=3,反应方程式为:X(g)+4Y(g)?2Z(g)+3Q(g),
(1)2min内生成0.1molX,根据反应X(g)+4Y(g)?2Z(g)+3Q(g)可知,2min内生成Y的物质的量为0.4mol,则起始时Y的物质的量为:2.7mol-0.4mol=2.3mol;
Q在2min内物质的量减少,根据反应方程式可知,2min内消耗的Q的物质的量为:0.1mol×3=0.3mol,则起始是Q的物质的量为:2.7mol+0.3mol=3mol,
故答案为:2.3mol;3mol;
(2)根据以上分析可知,m=1、n=4、p=2、q=3,故答案为:1;
(3)2min内消耗的Z的物质的量为:n(Z)=1mol-0.8mol=0.2mol,
则用Z表示2min内的反应速率为:v(Z)=$\frac{\frac{0.2mol}{2L}}{2min}$=0.05mol•L-1•min-1,
故答案为:0.05mol•L-1•min-1;
(4)2min内v(Q)=0.075mol•L-1•min-1,则△n(Q)=0.075mol•L-1•min-1×2min×2=0.3mol,
根据(1)可知反应前Q的物质的量为3mol,
所以2min末Q的转化率为:$\frac{0.3mol}{3mol}$×100%=10%,
故答案为:10%.
点评 本题考查较为综合,涉及化学反应速率、化学平衡的计算,题目难度中等,试题涉及的内容较多,考查比较全面,明确反应速率与化学计量数的关系为解答关键,注意掌握化学反应速率的概念及计算方法.

 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案| A. | 当b>2a时,发生的离子反应为:CO32-+2H+=H2O+CO2↑ | |
| B. | 当b<a时,发生的离子反应为:CO32-+H+=HCO3- | |
| C. | 当4a=3b时,发生的离子反应为:3CO32-+4H+=2HCO3-+CO2↑+H2O | |
| D. | 当a<b<2a时,反应生成的HCO3-与CO2的物质的量之比为(b-a):(2b-a) |
| 实验编号 | 反应条件 | 时间 | NO/mol | Cl2/mol | NOCl/mol |
| 实验① | T、恒容 | 初始 | 0.2 | 0.1 | 0 |
| 10 min | 0.05 | 0.025 | |||
| 12 min | 0.15 | ||||
| 实验② | T、恒压 | 初始 | 0.2 | 0.1 | 0 |
| A. | 实验①中,0~10min内,v(NOCl)=7.5×10-3 mol•L-1•min-1 | |
| B. | 平衡时若升高温度,达到新平衡时K=400,则该反应△H>0 | |
| C. | 平衡时实验②比实验①的Cl2转化率大 | |
| D. | 若实验①起始只充入0.4molNOCl,则平衡时NOCl浓度大于0.15mol•L-1 |
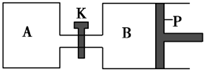 如图所示的装置中发生反应2A2(g)+B2(g)?2C(g)△H=-a kJ•mol-1(a>0),已知P是可自由滑动的活塞.在相同温度时关闭K,向A、B容器中分别充入2mol A2和1mol B2,两容器分别在500℃时达平衡,A中C的浓度为w1 mol•L-1,放出热量b kJ,B中C的浓度为w2 mol•L-1,放出热量c kJ.下列说法错误的是( )
如图所示的装置中发生反应2A2(g)+B2(g)?2C(g)△H=-a kJ•mol-1(a>0),已知P是可自由滑动的活塞.在相同温度时关闭K,向A、B容器中分别充入2mol A2和1mol B2,两容器分别在500℃时达平衡,A中C的浓度为w1 mol•L-1,放出热量b kJ,B中C的浓度为w2 mol•L-1,放出热量c kJ.下列说法错误的是( )| A. | 此反应的平衡常数表达式为K=$\frac{{c}^{2}(C)}{{c}^{2}({A}_{2})•c({B}_{2})}$ | |
| B. | C的浓度大小比较为:w2<w1 | |
| C. | a、b、c由大到小的关系为a>c>b | |
| D. | 若打开K,一段时间后重新达平衡,容器B的体积将减小 |
| 时间/s | 20 | 40 | 60 | 80 | 100 |
| c(NO2 )/(mol/L) | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
(1)20s内,v(NO2)=0.006mol•L-1•s-1.
(2)升高温度时,气体颜色加深,则正反应是吸热(填“放热”或“吸热”)反应.
(3)该温度下反应的化学平衡常数数值为1.8.
(4)相同温度下,若开始时向该容器中充入的是0.20molN2O4和0.40molNO2,则达到平衡后,c(NO2)=0.30mol/L.
