题目内容
下列反应的离子方程式书写正确的是( )
| A、向明矾溶液中加入等物质的量的Ba(OH)2溶液Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
| B、向Fe2(SO4)3溶液中通入足量的H2S:Fe3++H2S=Fe2++S↓+2H+ |
| C、向硝酸银溶液中滴加过量氨水:Ag++2NH3?H2O=[Ag(NH3)2]++2H2O |
| D、含等物质的量的硫酸氢铵与氢氧化钠两种溶液混合:NH4++HSO4-+2OH-=SO42-+NH3↑+2H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.3molBa(OH)2与3molKAl(SO4)2反应生成硫酸钡、硫酸铝和硫酸钾;
B.电荷不守恒;
C.向硝酸银溶液中滴加过量氨水,发生络合反应生成银氨络合溶液;
D.含等物质的量的硫酸氢铵与氢氧化钠两种溶液混合,反应实质为氢离子与氢氧根离子反应生成水.
B.电荷不守恒;
C.向硝酸银溶液中滴加过量氨水,发生络合反应生成银氨络合溶液;
D.含等物质的量的硫酸氢铵与氢氧化钠两种溶液混合,反应实质为氢离子与氢氧根离子反应生成水.
解答:
解:A.向明矾溶液中加入等物质的量的Ba(OH)2溶液,离子方程式为:2Al3++3SO42-+3Ba2++6OH-=3Al(OH)3↓+3BaSO4↓,故A错误;
B.向Fe2(SO4)3溶液中通入足量的H2S,离子方程式为:2Fe3++H2S=2Fe2++S↓+2H+,故B错误;
C.向硝酸银溶液中滴加过量氨水,离子方程式:Ag++2NH3?H2O=[Ag(NH3)2]++2H2O,故C正确;
D.含等物质的量的硫酸氢铵与氢氧化钠两种溶液混合,离子方程式:OH-+H+=H2O,故D错误;
故选:C.
B.向Fe2(SO4)3溶液中通入足量的H2S,离子方程式为:2Fe3++H2S=2Fe2++S↓+2H+,故B错误;
C.向硝酸银溶液中滴加过量氨水,离子方程式:Ag++2NH3?H2O=[Ag(NH3)2]++2H2O,故C正确;
D.含等物质的量的硫酸氢铵与氢氧化钠两种溶液混合,离子方程式:OH-+H+=H2O,故D错误;
故选:C.
点评:本题考查了离子方程式的书写,明确反应的实质是解题关键,注意反应物用量对反应的影响,选项AD为易错选项.

练习册系列答案
相关题目
某无色溶液中加入氢氧化铝,氢氧化铝迅速溶解,则该溶液中一定能够大量共存的离子组是( )
| A、K+、Na+、SO42-、Cl- |
| B、Na+、NH4+、SO42-、Cl- |
| C、Na+、K+、SO32-、NO3- |
| D、Na+、K+、MnO4-、Br- |

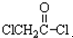 与足量的NaOH溶液共热充分反应的化学方程式:
与足量的NaOH溶液共热充分反应的化学方程式: