题目内容
14.光照条件下,1mol CH4与足量氯气充分反应,反应产物的物质的量最多的是( )| A. | CH3Cl | B. | CH2Cl2 | C. | CHCl3 | D. | HCl |
分析 光照条件下,CH4与足量氯气充分反应发生的反应方程式有CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl、CH3Cl+Cl2$\stackrel{光照}{→}$CH2Cl2+HCl、CH2Cl2+Cl2$\stackrel{光照}{→}$CHCl3+HCl、CHCl3+Cl2$\stackrel{光照}{→}$CCl4+HCl,无论发生哪一步反应都生成HCl,据此分析解答.
解答 解:光照条件下,CH4与足量氯气充分反应发生的反应方程式有CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl、CH3Cl+Cl2$\stackrel{光照}{→}$CH2Cl2+HCl、CH2Cl2+Cl2$\stackrel{光照}{→}$CHCl3+HCl、CHCl3+Cl2$\stackrel{光照}{→}$CCl4+HCl,根据方程式知,无论发生哪一步反应都生成HCl,所以反应产物的物质的量最多的是HCl,故选D.
点评 本题考查甲烷的取代反应,为高频考点,明确取代反应特点是解本题关键,注意:甲烷和氯气反应时被取代H原子与氯气分子关系式,为易错点.

练习册系列答案
相关题目
4.一定温度下在容积恒定的密闭容器中,进行如下可逆反应:A(g)+2B(g)═C(g)+D(g),当下列物理量不再发生变化时,不能表明该反应达到平衡状态的是( )
| A. | 混合气体密度 | B. | 容器内气体的压强 | ||
| C. | 混合气体的平均相对分子质量 | D. | A的转化率 |
5.除去下列括号内杂质的试剂或方法错误的是( )
| A. | MgO固体(SiO2),加过量NaOH溶液充分反应,过滤、洗涤、干燥 | |
| B. | CO2(SO2),酸性KMnO4溶液、浓硫酸,洗气 | |
| C. | KNO3晶体(NaCl),蒸馏水溶解、蒸发、结晶、过滤、洗涤、干燥 | |
| D. | FeCl3溶液(CuCl2),过量铁粉,过滤 |
2.对于下列事实的解释错误的是( )
| A. | 浓硫酸使胆矾晶体的蓝色褪去,说明浓硫酸具有吸水性 | |
| B. | 豆科植物根部的根瘤菌可以将空气中的氮由游离态转为化合态是氮的固定 | |
| C. | 常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应 | |
| D. | 氨水可使酚酞试剂变为红色,说明氨水显碱性 |
9.已知几种共价键能数据如下:
(1)通过计算,写出合成氨反应的热化学方程式:N2(g)+3H2(g)?2NH3(g)△H=-90.8kJ/mol.
(2)某温度下,以0.1mol N2和0.4mol H2作为初始反应物,在体积为2L的恒容密闭容器中进行合成氨反应,5min后测得反应放热2270J.则此时容器中N2的物质的量浓度c(N2)=0.0375mol/L,用H2表示的化学反应速率v(H2)=0.0075mol•L-1min-1.
| 共价键 | N≡N | H-H | N-H |
| 键能(kJ/mol) | 946 | 436 | 390.8 |
(2)某温度下,以0.1mol N2和0.4mol H2作为初始反应物,在体积为2L的恒容密闭容器中进行合成氨反应,5min后测得反应放热2270J.则此时容器中N2的物质的量浓度c(N2)=0.0375mol/L,用H2表示的化学反应速率v(H2)=0.0075mol•L-1min-1.
8.常温下,不能证明HA是弱酸的是( )
| A. | NaA的溶液呈碱性 | B. | pH=2的HA溶液稀释100倍后pH=3.5 | ||
| C. | 0.01 mol•Lˉ1HA溶液的pH=4 | D. | HA溶液跟锌反应,放出H2很慢 |
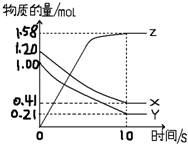 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
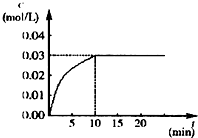 在某一容积为5L的密闭容器内,加入 0.2mol的CO和0.2mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),△H<0,反应中CO2的浓度随时间变化情况如图:
在某一容积为5L的密闭容器内,加入 0.2mol的CO和0.2mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),△H<0,反应中CO2的浓度随时间变化情况如图: