题目内容
现有Mg、Al、Zn三中金属组成的混合物,与足量的稀硫酸反应,产生气体3.36L(标准状况下),则合金的质量可能是( )
| A、2.5g |
| B、5.0 g |
| C、10.0g |
| D、12.5g |
考点:有关混合物反应的计算
专题:
分析:Mg、Zn与盐酸反应都表现为+2价,Al与盐酸反应表现+3价,可把Mg、Zn看成一种成分,Al看成另一种成分,则把该混合物转化成+2价的金属和+3价的金属组成的混合物,然后用极端法计算,假设全部是Mg(Zn),假设全是Al,计算Mg、Al物质的量,实际混合物的质量之和应介于二者之间.
解答:
解:氢气的物质的量=
=0.15mol,
假设全部是Mg或Zn,设它们的物质的量之和为xmol,产生的H2有如下关系:
Mg(Zn)~H2
1mol 1mol
x 0.15mol
所以,1mol:1mol=xmol:0.15mol,解得x=0.15
假设全是Al,设它的物质的量为ymol,产生的H2关系为:
2 Al~3H2
2mol 3mol
y 0.15mol
所以,2mol:3mol=ymol:0.15mol,解得y=0.1,所以固体质量在0.15mol×65g/mol=9.75g和0.1mo×27g/mol=2.7g之间,选项中只有B符合,
故选B.
| 3.36L |
| 22.4L/mol |
假设全部是Mg或Zn,设它们的物质的量之和为xmol,产生的H2有如下关系:
Mg(Zn)~H2
1mol 1mol
x 0.15mol
所以,1mol:1mol=xmol:0.15mol,解得x=0.15
假设全是Al,设它的物质的量为ymol,产生的H2关系为:
2 Al~3H2
2mol 3mol
y 0.15mol
所以,2mol:3mol=ymol:0.15mol,解得y=0.1,所以固体质量在0.15mol×65g/mol=9.75g和0.1mo×27g/mol=2.7g之间,选项中只有B符合,
故选B.
点评:本题考查混合物的计算,难度中等,注意根据化合价将三组分看做二组分,再采取极端法解答,极端法是化学计算中的一种技巧性解法,对于混合物范围计算比较适用,该方法的解题思路是假设只有混合物中的某一成份,通过计算得出两个极端值.

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案 课课练江苏系列答案
课课练江苏系列答案
相关题目
下列叙述错误的是( )
| A、制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中的乙酸 |
| B、SO2使溴水褪色与乙烯使KMnO4溶液褪色的原理相同 |
| C、用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率 |
| D、用AgNO3溶液可以鉴别KCl和KI |
常温下,若溶液由pH=3的HA溶液V1 mL与pH=11的NaOH溶液V2mL混合而得,则下列说法正确的是 ( )
| A、若反应后溶液呈中性,则c(H+)+c(OH-)=2×10-7mol?L-1 |
| B、若V1=V2,反应后溶液的pH一定等于7 |
| C、若反应后溶液呈酸性,则V1一定大于V2 |
| D、若反应后溶液呈碱性,则V1一定小于V2. |
关于原子核外电子运动及描述的说法,不正确的是( )
| A、氢原子核外电子云图,表示氢原子的核外电子的运动轨迹 |
| B、多电子原子核外电子,是按照电子的能量由低到高的顺序,从近到远排列 |
| C、多电子原子核外电子可以根据其能量不同分成K、L、M、N …等不同的能层 |
| D、从第二能层开始,每个能层里面又可以分成几个能级,如s、p、d、f…等 |
下列实验误差分析错误的是( )
| A、用湿润的pH试纸测稀碱溶液的pH,测定值偏小 |
| B、用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 |
| C、滴定前滴定管尖嘴内有气泡,终点读数时尖嘴内无气泡,所测体积偏大 |
| D、测定1mol气体体积时,未冷却至室温就读数,所测体积偏大 |
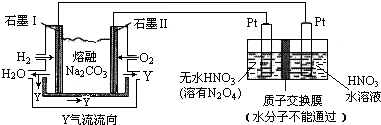
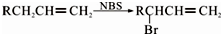 .
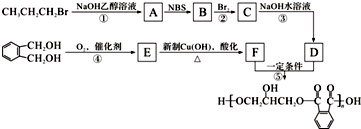
.
 的同分异构体中同时符合下列条件的芳香族化合物共有
的同分异构体中同时符合下列条件的芳香族化合物共有