题目内容
1.将一块质量为8.5g的铁合金(成分为铁和碳)放入烧杯中,再向烧杯中加入91.9g稀H2SO4,恰好与铁合金中的铁完全反应(碳不溶于稀H2SO4),所得氢气的质量为0.3g.已知含碳量高于2%的铁合金为生铁,含碳量低于2%的铁合金为钢,试根据计算回答:(1)该铁合金是生铁还是钢?
(2)反应后所得溶液中溶质的质量分数是多少?
分析 (1)由生成氢气的质量和铁合金的质量,根据铁与稀硫酸反应的化学方程式可以计算出铁合金中铁的质量和生成硫酸亚铁的质量;铁合金的质量与铁的质量之差就是铁合金中碳的质量,碳的质量与铁合金的质量之比就是铁合金的含碳量.通过比较就可以知道是生铁还是钢.
(2)由铁的质量加上稀硫酸的质量去掉生成氢气的质量,就是所得溶液的质量;硫酸亚铁的质量与所得溶液的质量之比就是所得溶液中溶质的质量分数.
解答 解:设铁合金中铁的质量为x,生成硫酸亚铁的质量为y.
Fe+H2SO4=FeSO4+H2↑
56 152 2
x y 0.3g
则:$\frac{56}{x}$=$\frac{152}{y}$=$\frac{2}{0.3g}$,
解得:x=8.4g、y=22.8g,
(1)铁合金的含碳量为:$\frac{8.5g-8.4g}{8.5g}$×100%≈1.2%<2%,故该铁合金属于钢,
答:通过计算可知该合金是钢;
(2)反应后溶液中溶质的质量分数为:$\frac{22.8g}{8.4g+91.9g-0.3g}$×100%=22.8%,
答:反应后所得溶液中溶质的质量分数是22.8%.
点评 本题考查混合物反应的计算,题目难度中等,明确发生反应的原理为解答关键,注意掌握质量分数的概念及计算方法,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
6.下列说法正确的是( )
| A. | 常温下,将pH=2的HA溶液与pH=12的BOH溶液等体积混合后,溶液的pH<7,则BA为强酸弱碱盐 | |
| B. | 弱电解质溶液稀释后,溶液中各离子浓度一定都减小 | |
| C. | 常温下,向体积相同pH均为1的盐酸和醋酸溶液中分别加入足量锌片,两种溶液生成H2的体积相同 | |
| D. | 常温下,将pH均为13的NaOH溶液和氨水分别加水稀释100倍后,氨水的碱性强于NaOH溶液 |
10.NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,2.24LO2中含有的共键数为0.4NA | |
| B. | 0.1molH2S和0.1molSO2混合后,体系中的硫原子数0.2NA | |
| C. | 100g质量分数为16.2%HBr溶液中的氢原子数为NA | |
| D. | 3.9gNa2O2晶体中所含的离子总数为0.5NA |
11.已知标准状况下5.6LX气体的质量为8g,则X气体的摩尔质量是( )
| A. | 16g | B. | 32g | C. | 64g/mol | D. | 32g/mol |
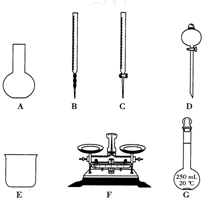 某化学兴趣小组测定某FeCl3样品(含少量FeCl2杂质)中铁元素的质量分数,实验按以下步骤进行:①称取ag样品,置于烧杯中;②加入适量盐酸和适量蒸馏水,使样品溶解,然后准确配制成250mL溶液;③准确量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,使反应完全;④加入过量氨水,充分搅拌,使沉淀完全;⑤过滤,洗涤沉淀;⑥将沉淀转移到坩埚内,加热、搅拌,直到固体由红褐色全部变为红棕色后,在干燥器中冷却至室温后,称量;⑦…
某化学兴趣小组测定某FeCl3样品(含少量FeCl2杂质)中铁元素的质量分数,实验按以下步骤进行:①称取ag样品,置于烧杯中;②加入适量盐酸和适量蒸馏水,使样品溶解,然后准确配制成250mL溶液;③准确量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,使反应完全;④加入过量氨水,充分搅拌,使沉淀完全;⑤过滤,洗涤沉淀;⑥将沉淀转移到坩埚内,加热、搅拌,直到固体由红褐色全部变为红棕色后,在干燥器中冷却至室温后,称量;⑦…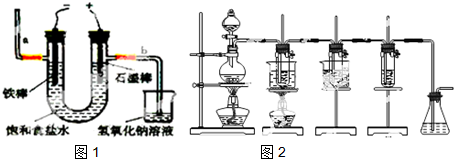
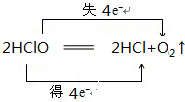 .
.