题目内容
 某溶液中含有Ba2+、Cu2+、Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离.
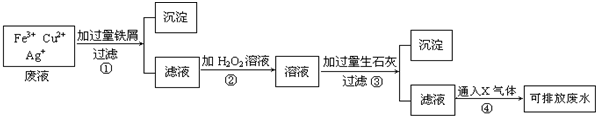
某溶液中含有Ba2+、Cu2+、Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离.其流程如图,已知沉淀2为蓝色.
(1)沉淀的化学式:沉淀1
(2)写出混合液+A的离子方程式
考点:常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题
分析:溶液含有Ba2+、Cu2+、Ag+,应先加入HCl,生成AgCl沉淀,过滤后再加入NaOH得到Cu(OH)2沉淀,最后加入Na2SO4,可得到BaSO4沉淀,根据物质的性质书写反应的离子方程式.
解答:
解:(1)溶液含有Ba2+、Cu2+、Ag+,应先加入HCl,生成AgCl沉淀,过滤后再加入NaOH得到Cu(OH)2沉淀,最后加入Na2SO4,可得到BaSO4沉淀,所以沉淀1是氯化银,沉淀2是氢氧化铜,沉淀3是硫酸钡,故答案为:AgCl;BaSO4;
(2)混合液+A反应的离子方程式为Ag++Cl-=AgCl↓,沉淀2为Cu(OH)2,溶液+B反应的离子方程式为:Cu2++2OH-=Cu(OH)2↓,
故答案为:Ag++Cl-=AgCl↓;Cu2++2OH-=Cu(OH)2↓.
(2)混合液+A反应的离子方程式为Ag++Cl-=AgCl↓,沉淀2为Cu(OH)2,溶液+B反应的离子方程式为:Cu2++2OH-=Cu(OH)2↓,
故答案为:Ag++Cl-=AgCl↓;Cu2++2OH-=Cu(OH)2↓.
点评:本题考查离子方程式的书写,题目难度中等,注意使离子逐一沉淀应先加入HCl,不能先加入NaOH,否则不能达到逐一沉淀的目的.

练习册系列答案
相关题目
只由KHS、CaSO4、KHSO3、CaSO3四种物质组成的固体粉末中,测知硫元素的质量分数ω(S)=a%,则氧元素的质量分数ω(O)为( )
| A、1-2.25a% |
| B、2.25a% |
| C、1-1.75a% |
| D、全部 |
下列说法正确的是:①明矾晶体是混合物②BaSO4是一种难溶于水的电解质③硫酸、纯碱、小苏打分别属于酸、碱、盐④氧化还原反应都属于离子反应⑤酸雨是指pH小于7.0的降水⑥丁达尔效应可以区分溶液和胶体.其中正确的是( )
| A、①②⑥ | B、①④⑤ |
| C、③④ | D、②⑥ |
下列离子检验的方法正确的是( )
| A、某溶液+AgNO3溶液→生成白色沉淀,说明原溶液中有Cl- |
| B、某溶液+BaCl2溶液→生成白色沉淀,说明原溶液中有SO42- |
| C、某溶液+NaOH溶液→生成蓝色沉淀,说明原溶液中有Cu2+ |
| D、某溶液+稀硫酸→产生无色气体,该气体能使澄清石灰水变浑浊,则原溶液中有CO32- |
关于下图所示实验装置的叙述错误的是( )


| A、将水准管上提,液面高于量气管且不下降,说明装置不漏气 |
| B、若已知参加反应的Zn的质量,则该装置可用来测定气体摩尔体积 |
| C、若已知参加反应的Zn的质量,则该装置可用来测定锌的相对原子质量 |
| D、反应停止后,立即读数 |
实验室需用240mL 0.1mol?L-1的硫酸铜溶液,现选取250mL容量瓶进行配制,以下操作能配制成功的是( )
| A、称取3.84 g CuSO4粉末,加入250 mL水 |
| B、称取6.25 g CuSO4?5H2O晶体,加水配成250 mL溶液 |
| C、称取4.0 g CuSO4粉末,加入250 mL水 |
| D、称取4.0 g CuSO4?5H2O晶体,加水配成250 mL溶液 |