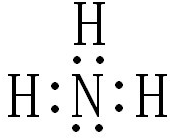题目内容
16.将铜片放入盛有足量稀硫酸的烧杯中,若使铜片溶解,则不能在烧杯中加入( )| A. | 三氯化铁固体 | B. | 硝酸铵固体 | C. | 稀硝酸溶液 | D. | 硫酸亚铁固体 |
分析 铜与稀硫酸不反应,加入某种物质后能溶解,说明所加物质能够直接氧化金属铜或在酸性条件下具有强氧化性,据此进行解答.
解答 解:A.加入氯化铁固体后,铁离子与金属铜发生反应生成亚铁离子和铜离子,导致铜溶解,故A错误;
B.加入硝酸铵后,硝酸根离子在酸性条件下具有强氧化性,能够氧化铜,导致铜溶解,故B错误;
C.加入稀硝酸后,稀硝酸具有强氧化性,能够氧化铜,导致铜溶解,故C错误;
D.加入硫酸亚铁后,铜与硫酸亚铁不反应,铜不会溶解,故D正确;
故选D.
点评 本题考查了常见金属及其化合物性质,题目难度中等,明确硝酸根离子在酸性条件下具有强氧化性为解答关键,注意掌握常见金属单质及其化合物性质,试题培养了学生的灵活应用能力.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
6.下列各组离子,可以形成无色透明碱性溶液的是( )
| A. | K+、NH4+、OH-、NO3- | B. | Mg2+、Na+、AlO2-、OH- | ||
| C. | Na+、Ba2+、OH-、SO42- | D. | Cu2+、Al3+、SO42-、Cl- |
7.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=1012的溶液中:K+、Cl-、NO3-、Fe3+ | |
| B. | 能使甲基橙显红色的溶液:CO32-、Na+、Cl-、SO42- | |
| C. | pH=1的溶液中:Mg2+、SO42-、Fe2+、Cu2+ | |
| D. | 能使铝钝化的溶液中:Ba2+、Na+、Cl-、I- |
4.高中化学学习过程中的物质颜色是需要注意的.下列关于颜色的描述正确的个数是( )
①氯水放久了会逐渐由黄绿色变成几乎无色
②用硝酸银检验Br-会产生AgBr难溶于水的白色沉淀
③KI溶液中加入淀粉溶液会变成蓝色
④溴水中加入CCl4振荡静置后,上层为橙红色
⑤实验室的浓硝酸溶液久置呈黄色.
①氯水放久了会逐渐由黄绿色变成几乎无色
②用硝酸银检验Br-会产生AgBr难溶于水的白色沉淀
③KI溶液中加入淀粉溶液会变成蓝色
④溴水中加入CCl4振荡静置后,上层为橙红色
⑤实验室的浓硝酸溶液久置呈黄色.
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
11.用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 22.4 L N2和NH3混合气体中原子间共有3NA个共用电子对 | |
| B. | 3.0 g甲醛HCHO和乙酸混合物中共含碳原子数为0.1NA | |
| C. | 25℃时pH=1的醋酸溶液中含有H+的数目为0.1NA | |
| D. | 标准状况下,2.24 L CH2Cl2含有的分子数为0.1NA |
5.有可逆反应C(s)+H2O(g)?H2(g)+CO(g)处于平衡状态,当平衡向左移动时,混合气体相对平均分子质量变化正确的是下列选项中的( )
| A. | 增大 | B. | 减小 | C. | 不变 | D. | 前三种均有可能 |
6.下列清洗仪器的方法及相关离子方程式不正确的是( )
| A. | 用稀盐酸清洗装石灰水的试剂瓶:CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | 用稀盐酸清洗试管中的二氧化锰:MnO2+4H++2Cl-═Mn2++Cl2↑+2H2O | |
| C. | 用稀硝酸溶解试管中的银镜:3Ag+NO3-+4H+═3Ag++NO↑+2H2O | |
| D. | 用稀硫酸清洗试管中的氧化铜:CuO+2H+═Cu2++H2O |
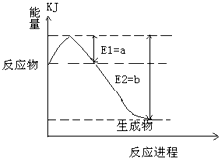 合成氨工业对国民经济和社会发展具有重要意义
合成氨工业对国民经济和社会发展具有重要意义