题目内容
20mL0.5mol/LAlCl3溶液与10mL3mol/LNaCl溶液中的Cl-的物质的量浓度之比为 .
考点:物质的量浓度的相关计算
专题:
分析:1molAlCl3电离产生3molCl-,氯化铝溶液中Cl-的物质的量浓度为氯化铝的3倍,1molNaCl电离产生1molCl-,NaCl溶液中的Cl-的物质的量浓度等于氯化钠的浓度.
解答:
解:20mL0.5mol/LAlCl3溶液中Cl-的物质的量浓度为0.5mol/L×3=1.5mol/L,
10mL3mol/LNaCl溶液中Cl-的物质的量浓度为3mol/L×1=3mol/L
故二者溶液Cl-的物质的量浓度之比为1.5mol/L:3mol/L=1:2,
故答案为:1:2.
10mL3mol/LNaCl溶液中Cl-的物质的量浓度为3mol/L×1=3mol/L
故二者溶液Cl-的物质的量浓度之比为1.5mol/L:3mol/L=1:2,
故答案为:1:2.
点评:本题考查物质的量浓度有关计算,比较基础,注意对基础知识的理解掌握.

练习册系列答案
相关题目
常温常压下,0.1mol两种气态烃组成的混合物完全燃烧后得到0.16mol二氧化碳和3.6g水,则混合气体中( )
| A、一定有甲烷 |
| B、一定有丙烯 |
| C、一定有乙炔 |
| D、一定有乙烷 |
在一密闭容器中充入一定量的N2和H2,发生反应N2(g)+3H2(g)?2NH3(g)经测定反应开始后的2s内氢气的平均速率:ν(H2)=0.45mol/(L?s),则2s末NH3的浓度为( )
| A、0.50mol/L |
| B、0.60mol/L |
| C、0.45mol/L |
| D、0.55mol/L |
已知1mol红磷转化为1mol白磷,吸收18.39kJ热量.①4P(s,红)+5O2(g)═2P2O5(s)△H1 ②4P(s,白)+5O2(g)═2P2O5(s)△H2,则△H1与△H2的关系正确的是( )
| A、△H1=△H2 |
| B、△H1>△H2 |
| C、△H1<△H2 |
| D、无法确定 |
某反应过程能量变化如图所示,下列说法不正确的是( )
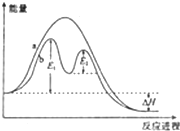

| A、反应过程b有催化剂参与 |
| B、该反应为放热反应,热效应等于△H |
| C、加入催化剂,可改变该反应的活化能 |
| D、有催化剂的条件下,反应的活化能等于E1+E2 |
下列过程中△H大于零的是( )
| A、氢氧化钡晶体与氯化铵固体反应 |
| B、甲烷燃烧 |
| C、氢氧化钠与稀硝酸反应 |
| D、实验室用Zn与稀硫酸制备氢气 |
下列元素中,基态原子的外围电子排布式不正确的是( )
| A、As 4s24p3 |
| B、Cr 3d44s2 |
| C、Ar 3s23p6 |
| D、Fe 3d64s2 |
金属钠在空气中长久放置,最终生成物是( )
| A、Na2O2 |
| B、Na2O |
| C、Na2CO3 |
| D、NaOH |