题目内容
已知:CH3(CH2)2CH3(g)+
O2(g)═4CO2(g)+5H2O(l);△H=-2878kJ?mol-1
(CH3)2CHCH3(g)+
O2(g)═4CO2(g)+5H2O(l);△H=-2869kJ?mol-1
下列说法正确的是( )
| 13 |
| 2 |
(CH3)2CHCH3(g)+
| 13 |
| 2 |
下列说法正确的是( )
分析:A、根据烷烃的结构特征分析解决,烷烃分子中碳原子都是以单键和其他原子连接;
B、根据热化学方程式中的定量关系计算比较;
C、根据题给热化学方程式和燃烧热的概念分析判断;
D、由题给热化学方程式两式相减得到异丁烷转化为正丁烷的热化学方程式即可做出判断.
B、根据热化学方程式中的定量关系计算比较;
C、根据题给热化学方程式和燃烧热的概念分析判断;
D、由题给热化学方程式两式相减得到异丁烷转化为正丁烷的热化学方程式即可做出判断.
解答:解:A、等量的正丁烷和异丁烷是同分异构体,都是烷烃,烷烃中碳原子形成的化学键都是单键,所以分子内有多少个氢原子,就会有多少个碳氢键,所以二者所含碳氢键相同,故A错误;
B、热化学方程式相减得到CH3CH2CH2CH3(g)═(CH3)2CHCH3(g)△H=-9kJ?mol-1,此过程是一个放热过程,所以正丁烷能量高于异丁烷,故B错误;
C、燃烧热是1mol物质完全燃烧生成稳定氧化物放出热量,热化学方程式是两种可燃物质的燃烧热,正丁烷的燃烧热△H=-2878kJ?mol-1,故C正确;
D、热化学方程式相减得到(CH3)2CHCH3(g)═CH3CH2CH2CH3(g)△H=9kJ?mol-1,异丁烷转化为正丁烷的过程是一个吸热过程,故D错误;
故选:C.
B、热化学方程式相减得到CH3CH2CH2CH3(g)═(CH3)2CHCH3(g)△H=-9kJ?mol-1,此过程是一个放热过程,所以正丁烷能量高于异丁烷,故B错误;
C、燃烧热是1mol物质完全燃烧生成稳定氧化物放出热量,热化学方程式是两种可燃物质的燃烧热,正丁烷的燃烧热△H=-2878kJ?mol-1,故C正确;
D、热化学方程式相减得到(CH3)2CHCH3(g)═CH3CH2CH2CH3(g)△H=9kJ?mol-1,异丁烷转化为正丁烷的过程是一个吸热过程,故D错误;
故选:C.
点评:本题考查了热化学方程式的应用,物质的能量高低比较,有机物分子结构的判断等知识.

练习册系列答案
相关题目
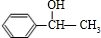
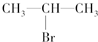 (主要产物),1mol某烃A充分燃烧后可以得到8mol CO2和4mol H2O.该烃A在不同条件下能发生如下所示的一系列变化.
(主要产物),1mol某烃A充分燃烧后可以得到8mol CO2和4mol H2O.该烃A在不同条件下能发生如下所示的一系列变化.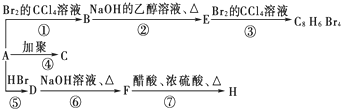
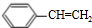
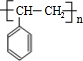
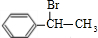
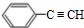
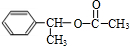
 +NaBr
+NaBr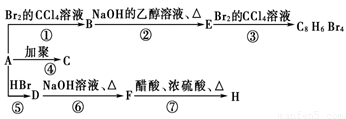
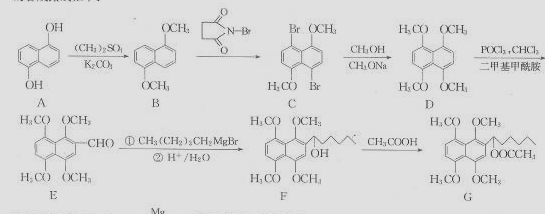
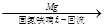 CH3(CH2)3CH2MgBr
CH3(CH2)3CH2MgBr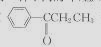 )的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:CH3CH2OH
)的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:CH3CH2OH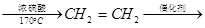
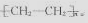
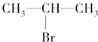 (主要产物),1mol某烃A充分燃烧后可以得到8mol CO2和4mol H2O.该烃A在不同条件下能发生如下所示的一系列变化.
(主要产物),1mol某烃A充分燃烧后可以得到8mol CO2和4mol H2O.该烃A在不同条件下能发生如下所示的一系列变化.