题目内容
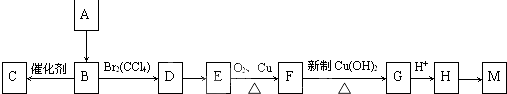
 现有A、B、C三种物质,均含同一种元素,一定条件下其转化关系如下(部分产物已略去):
现有A、B、C三种物质,均含同一种元素,一定条件下其转化关系如下(部分产物已略去):请回答:
(1)若A是短周期元素组成的金属单质,D是短周期中原子半径最大的主族元素形成的氢氧化物.
①组成A的元素在周期表中的位置是
②当A与D的溶液反应转移1.5mol电子时,产生气体的体积(标准状况)为
(2)若A是常见金属单质,B的溶液为黄色,D的组成元素的原子M层电子数比L层少1.
①下列关于C的说法正确的是
a.其溶液为无色
b.遇KSCN溶液变红色
c.既有氧化性也有还原性
d.其溶液可用于吸收氯气
②B与HI溶液反应可生成C、E和一种单质,该反应的化学方程式是
考点:无机物的推断
专题:
分析:(1)A、B、C三种物质,均含同一种元素,若A是短周期元素组成的金属单质,D是短周期中原子半径最大的主族元素形成的氢氧化物判断为NaOH,所以A为Al,B为NaAlO2,E为氧气,C为氧化铝;
①A为铝确定在周期表中的位置;
②铝与氢氧化钠溶液、反应生成偏铝酸钠和氢气;
(2)D的组成元素的原子M层电子数比L层少1,应为Cl2,B的溶液为黄色,应为FeCl3,则A为Fe,C为FeCl2,E为HCl,以此解答该题.
①A为铝确定在周期表中的位置;
②铝与氢氧化钠溶液、反应生成偏铝酸钠和氢气;
(2)D的组成元素的原子M层电子数比L层少1,应为Cl2,B的溶液为黄色,应为FeCl3,则A为Fe,C为FeCl2,E为HCl,以此解答该题.
解答:
解:(1)若A是常见金属单质,是短周期中原子半径最大的主族元素形成的氢氧化物,应含有Na元素,E为无色无味气体,是一种常见氧化剂,为O2,则C为金属氧化物,金属A和金属氧化物C都与Na的化合物反应,则A应为Al,C为Al2O3,D为NaOH,B为NaAlO2,
①组成A的元素在周期表中的位置是,故答案为:第三周期第IIIA族;
②A与D的溶液反应的方程式为2Al+2H2O+2OH-=2AlO2-+3H2↑,当2molAl参加反应时转移6mol 电子,生成3mol氢气,则转移1.5mol电子时,生成0.75mol电子,体积为0.75mol×22.4L/mol=16.8L,
故答案为:16.8L;2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)D的组成元素的原子M层电子数比L层少1,应为Cl2,B的溶液为黄色,应为FeCl3,则A为Fe,C为FeCl2,E为HCl,
①C为FeCl2,溶液呈浅绿色,Fe元素化合价为+2价,具有氧化性,可与活泼金属Mg、Zn等金属发生置换反应,具有还原性,可与氯气发生氧化还原反应,与KSCN溶液不发生显色反应,故答案为:cd;
②B为FeCl3,具有强氧化性,与HI反应的化学方程式为2FeCl3+2HI=2FeCl2+2HCl+I2,故答案为:2FeCl3+2HI=2FeCl2+2HCl+I2.
①组成A的元素在周期表中的位置是,故答案为:第三周期第IIIA族;
②A与D的溶液反应的方程式为2Al+2H2O+2OH-=2AlO2-+3H2↑,当2molAl参加反应时转移6mol 电子,生成3mol氢气,则转移1.5mol电子时,生成0.75mol电子,体积为0.75mol×22.4L/mol=16.8L,
故答案为:16.8L;2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)D的组成元素的原子M层电子数比L层少1,应为Cl2,B的溶液为黄色,应为FeCl3,则A为Fe,C为FeCl2,E为HCl,
①C为FeCl2,溶液呈浅绿色,Fe元素化合价为+2价,具有氧化性,可与活泼金属Mg、Zn等金属发生置换反应,具有还原性,可与氯气发生氧化还原反应,与KSCN溶液不发生显色反应,故答案为:cd;
②B为FeCl3,具有强氧化性,与HI反应的化学方程式为2FeCl3+2HI=2FeCl2+2HCl+I2,故答案为:2FeCl3+2HI=2FeCl2+2HCl+I2.
点评:本题考查无机物的推断,为高考常见题型,侧重于学生的分析能力和元素化合物知识的综合运用的考查,熟悉元素化合物知识是关键,题目难度中等,焰色反应以及气体的颜色为突破口.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g)?N2O5(g)+O2(g)有关说法正确的是( )
| A、升高温度可减小反应速率 |
| B、加入合适的催化剂可提高反应速率 |
| C、达到平衡时,v(正)=v(逆)=0 |
| D、达到平衡时,NO2转化率为100% |
化学与社会、生产、生活紧切相关,下列说法正确的是( )
| A、医疗上可用硫酸钡作x射线透视肠胃的内服药,是因为硫酸钡不溶于水 |
| B、酸雨指25℃时pH值小于7的降水 |
| C、加碘食盐中添加碘酸钾而不用碘化钾,是因为碘酸钾能溶于水而碘化钾不溶于水 |
| D、发酵粉能使焙制出的糕点疏松多孔,是因为发酵粉中含有碳酸氢钠 |
下列食用品的有效成分正确的是( )
A、 C6H12O6 |
B、 Na2CO3 |
C、 CH3COOH |
D、 Al(OH)3 |