题目内容
13.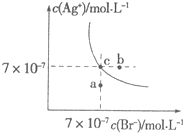 在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示.又知t℃时AgCl的Ksp=4×10-10,下列说法不正确的是( )
在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示.又知t℃时AgCl的Ksp=4×10-10,下列说法不正确的是( )| A. | 在t℃时,AgBr的Ksp为4.9×10-13 | |
| B. | 在AgBr饱和溶液中加入NaBr固体,可使溶液由c点到b点 | |
| C. | 图中a点对应的是AgBr的不饱和溶液 | |
| D. | 向组成为c点的溶液中加入等体积的0.1 mol/L的氯化钠溶液,可产生AgCl沉淀 |
分析 A.根据图中c点的c(Ag+)和c(Br-)可得该温度下AgBr的Ksp;
B.在AgBr饱和溶液中加入NaBr固体后,c(Br-)增大,溶解平衡逆向移动,c(Ag+)减小;
C.在a点时Qc=c(Ag+)•c(Br-)<Ksp,判断AgBr为不饱和溶液;
D.c点的溶液c(Ag+)=7×10-7mol/L,加入等体积的0.1 mol/L的氯化钠溶液,c(Ag+)、c(Cl-)分别为3.5×10-7mol/L、0.05mol/L,计算Qc,与Ksp比较可判断是否生成沉淀.
解答 解:A.结合图中c点的c(Ag+)和c(Br-)可知:该温度下AgBr的Ksp=7×10-7×7×10-7=4.9×10-13,故A正确;
B.在AgBr饱和溶液中加入NaBr固体后,c(Br-)增大,溶解平衡逆向移动,c(Ag+)减小,故B错误;
C.根据图象可知,在a点时Qc=c(Ag+)•c(Br-)<Ksp,所以a点为AgBr的不饱和溶液,故C正确;
D.c点的溶液c(Ag+)=7×10-7mol/L,加入等体积的0.1 mol/L的氯化钠溶液,c(Ag+)、c(Cl-)分别为3.5×10-7mol/L、0.05mol/L,c(Ag+)×c(Cl-)>Ksp,析出沉淀,故D正确.
故选B.
点评 本题考查了沉淀溶解平衡曲线,为高频考点,侧重考查学生的分析、计算能力,难度中等,曲线上的每个点都为AgBr饱和溶液,曲线以下为不饱和溶液;注意掌握Ksp的表达式及简单计算方法.

练习册系列答案
相关题目
18.对外加电流的金属保护中,被保护的金属( )
| A. | 与电源的正极相连 | B. | 表面上发生氧化反应 | ||
| C. | 与电源的负极相连 | D. | 与另一种活泼性较差的金属相连 |
19.下列有关有机化合物的说法正确的是( )
| A. | 乙烷室温下能与浓盐酸发生取代反应 | |
| B. | 由乙烯生成乙醇属于加成反应 | |
| C. | C4H9Cl有3种同分异构体 | |
| D. | 油脂和蛋白质都属于高分子化合物 |
1.常温下Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.0×10-16,将等体积的AgCl和AgI的饱和溶液的清液混合,再向其中加入一定量的AgNO3固体,下列说法正确的是( )
| A. | 若AgNO3足量,AgCl和AgI都可沉淀,但以AgCl为主 | |
| B. | 两清液混合,AgCl和AgI都沉淀 | |
| C. | 若取0.1435 g AgCl固体放入100mL水(忽略体积变化),c(Cl-)为0.01 mol/L | |
| D. | 向AgI清液加入AgNO3,c(Ag+)增大,Ksp(AgI)也增大 |
8. 常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水溶液中的沉淀溶解平衡曲线见如图.下列说法不正确的是( )
常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水溶液中的沉淀溶解平衡曲线见如图.下列说法不正确的是( )
 常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水溶液中的沉淀溶解平衡曲线见如图.下列说法不正确的是( )
常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水溶液中的沉淀溶解平衡曲线见如图.下列说法不正确的是( )| A. | CaSO4溶解在水中,c(Ca2+)=c(SO42-)=3×10-3mol/L | |
| B. | 在d点溶液中加入一定量的CaCl2可能会有沉淀析出 | |
| C. | a点对应的Ksp等于c点对应的Ksp | |
| D. | b点将有沉淀生成,平衡后溶液中c(SO42-)等于3×10-3mol/L |
18.已知常温下,KSP(AgCl)=1.8×10-10 mol2•L-2,KSP(AgI)=8.3×10-17mol2•L-2,下列叙述中,正确的是( )
| A. | 常温下,AgCl 在饱和 NaCl 溶液中的 KSP 比在纯水中的 KSP 小 | |
| B. | 向 AgCl 的悬浊液中加入 KI 溶液,沉淀由白色转化为黄色 | |
| C. | 将 0.001 mol•L-1 的 AgNO3 溶液滴入 KCl 和 KI 的混合溶液中,一定先产生 AgI 沉淀 | |
| D. | 向 AgCl 的饱和溶液中加入 NaCl 晶体,有 AgCl 析出且溶液中 c(Ag+)=c(Cl-) |
 有机化工原料溴乙烷的沸点为38.4℃.制备溴乙烷的一种方法是乙醇与氢溴酸反应,该反应的化学方程式是CH3CH2OH+HBr→CH3CH2Br+H2O.
有机化工原料溴乙烷的沸点为38.4℃.制备溴乙烷的一种方法是乙醇与氢溴酸反应,该反应的化学方程式是CH3CH2OH+HBr→CH3CH2Br+H2O.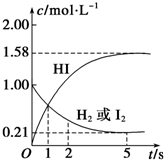 某温度时,向某V L的密闭容器中充入3molH2(g)和3mol I2(g),发生反应:
某温度时,向某V L的密闭容器中充入3molH2(g)和3mol I2(g),发生反应: