题目内容
阿伏加德罗常数为6.02×1023mol-1,下列说法中正确的是( )
| A、11.1mol?L-1CH3COOH溶液中,CH3COOH分子数约为6.02×1023 |
| B、常温常压下,N2和O2混合气体22.4L所含的分子数等于6.02×1023 |
| C、标准状况下,11.2L,CCl4所含的分子数约为3.01×1023 |
| D、含有0.01mol FeCl3的饱和FeCl3溶液滴于沸水中,继续煮沸,形成的红褐色Fe(OH)3胶体中含有的Fe(OH)3胶粒数目少于6.02×1023 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.醋酸为弱电解质,在溶液中部分电离,则溶液中醋酸的分子数减少;
B.常温常压下,不是标准状况下,不能使用标况下的气体摩尔体积计算混合气体的物质的量;
C.标准状况下,四氯化碳的状态为液体,不是气体;
D.氢氧化铁胶体粒子为氢氧化铁的聚集体,则氢氧化铁胶粒的数目小于铁离子数目.
B.常温常压下,不是标准状况下,不能使用标况下的气体摩尔体积计算混合气体的物质的量;
C.标准状况下,四氯化碳的状态为液体,不是气体;
D.氢氧化铁胶体粒子为氢氧化铁的聚集体,则氢氧化铁胶粒的数目小于铁离子数目.
解答:
解:A.11.1mol?L-1CH3COOH溶液中含有溶质醋酸1mol,由于醋酸部分电离,则溶液中醋酸分子的物质的量小于1mol,CH3COOH分子数约小于6.02×1023,故A错误;
B.常温常压下,不能使用标况下的气体摩尔体积计算22.4L混合气体的物质的量,故B错误;
C.标况下四氯化碳不是气体,不能使用标况下的气体摩尔体积计算11.2L四氯化碳的物质的量,故C错误;
D.氢氧化铁胶粒为氢氧化铁的聚集体,则0.01mol FeCl3的饱和FeCl3溶液滴于沸水中,继续煮沸,形成的红褐色Fe(OH)3胶体的物质的量小于0.01mol,含有的Fe(OH)3胶粒数目少于6.02×1021,更小于6.02×1023,故D正确;
故选D.
B.常温常压下,不能使用标况下的气体摩尔体积计算22.4L混合气体的物质的量,故B错误;
C.标况下四氯化碳不是气体,不能使用标况下的气体摩尔体积计算11.2L四氯化碳的物质的量,故C错误;
D.氢氧化铁胶粒为氢氧化铁的聚集体,则0.01mol FeCl3的饱和FeCl3溶液滴于沸水中,继续煮沸,形成的红褐色Fe(OH)3胶体的物质的量小于0.01mol,含有的Fe(OH)3胶粒数目少于6.02×1021,更小于6.02×1023,故D正确;
故选D.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确氢氧化铁胶粒为氢氧化铁的聚集体,要求掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项C为易错点,注意标况下四氯化碳不是气体.

练习册系列答案
相关题目
儿茶素(其结构简式如图所示)是茶叶的主要活性成分,具有抗氧化、抗菌、除臭等作用.下列说法正确的是( )
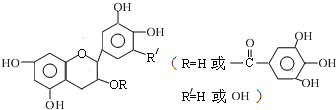

| A、常温下,儿茶素不溶于水,也不溶于有机溶剂 |
| B、儿茶素能与FeCl3溶液发生显色反应 |
| C、1mol儿茶素最多可与9mol NaOH反应 |
| D、儿茶素一定不能发生水解反应 |
工业上以铬铁矿(主要成分为FeO?Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7?2H2O),其主要反应为(1)4(FeO?Cr2O3)+8Na2CO3+7O2
8Na2CrO4+2Fe2O3+8CO2(2)2Na2CrO4+H2SO4═Na2SO4+Na2Cr2O7+H2O下列说法正确的是( )
| ||
| A、反应(1)和(2)均为氧化还原反应 |
| B、反应(1)中FeO?Cr2O3既是氧化剂又是还原剂 |
| C、高温下O2的氧化性大于Fe2O3小于Na2CrO4 |
| D、生成1mol的Na2Cr2O7时转移7mol电子 |
下列说法错误的是( )
| A、自然界中存在碳元素的单质,也存在硅元素的单质 |
| B、燃烧煤时加入适量的石灰石,可减少废气中二氧化硫的量 |
| C、利用丁达尔现象可以区分FeCl3溶液与Fe(OH)3胶体 |
| D、用焦炭在电炉中还原二氧化硅可得到含有少量杂质的粗硅 |
下列类型的反应中,生成物中肯定有单质的是( )
| A、化合反应 | B、分解反应 |
| C、置换反应 | D、复分解反应 |
 常温下,取pH=2的HA溶液与HB溶液各1mL,分别加水稀释,测得pH变化与稀释倍数关系如图所示.下列叙述正确的是( )
常温下,取pH=2的HA溶液与HB溶液各1mL,分别加水稀释,测得pH变化与稀释倍数关系如图所示.下列叙述正确的是( )| A、HB的电离方程式为HB═H++B- |
| B、稀释前,c(HB)>c(HA)=0.01mol?L-1 |
| C、NaA的水溶液中,离子浓度大小为c(Na+)>c(A-)>c(OH-)>c(H+) |
| D、NaA、NaB的混合溶液中:2c(Na+)=c(A-)+c(B-)+c(HB) |
设NA为阿伏加德罗常数的值,下列说法不正确的是( )
| A、标准状况下,22.4L的氖气含约NA个氖原子 |
| B、常温常压下,1mol氨气中含有10 NA个电子 |
| C、标准状况下,22.4L水中含有3 NA个原子核 |
| D、0.3mol?L-1的K2SO4溶液中含有K+和SO42-总数为0.9NA |
配制0.5mol/L的NaOH溶液1L,因操作不当使溶液浓度偏低的是( )
| A、用托盘天平称量20gNaOH时,使用生锈的砝码 |
| B、容量瓶中有少量的水 |
| C、定容时仰视容量瓶刻度线 |
| D、NaOH溶解后立即注入容量瓶中,洗涤、移液,并加蒸馏水定容至刻度线 |
下列叙述中,不正确的是( )
| A、Cl2和SO2分别通入品红试液中,均使品红试液褪色 |
| B、硝酸银溶液通常保存在棕色试剂瓶中 |
| C、常温下,铁和铝与浓硫酸不发生任何反应 |
| D、葡萄糖与新制的Cu(OH)2悬浊液反应,有砖红色物质生成 |