题目内容
水溶液中能大量共存的一组离子是( )
| A、Na+、Ca2+、Cl-、SO42- |
| B、Fe2+、H+、SO32-、ClO- |
| C、Mg2+、NH4+、Cl-、SO42- |
| D、K+、Fe3+、NO3-、SCN- |
考点:离子共存问题
专题:离子反应专题
分析:A.钙离子与硫酸根离子反应生成硫酸钙沉淀;
B.次氯酸根离子能够与氢离子反应生成次氯酸,次氯酸能够氧化亚硫酸根离子、亚铁离子;
C.四种离子之间不发生反应,在溶液中能够大量共存;
D.铁离子与硫氰根离子反应生成络合物硫氰化铁.
B.次氯酸根离子能够与氢离子反应生成次氯酸,次氯酸能够氧化亚硫酸根离子、亚铁离子;
C.四种离子之间不发生反应,在溶液中能够大量共存;
D.铁离子与硫氰根离子反应生成络合物硫氰化铁.
解答:
解:A.Ca2+、SO42-之间反应生成硫酸钙,在溶液中不能大量共存,故A错误;
B.ClO-与Fe2+、H+、SO32-发生反应,在溶液中不能大量共存,故B错误;
C.Mg2+、NH4+、Cl-、SO42之间不发生反应,在溶液中能够大量共存,故C正确;
D.Fe3+和SCN-之间反应生成络合物,在溶液中不能大量共存,故D错误;
故选C.
B.ClO-与Fe2+、H+、SO32-发生反应,在溶液中不能大量共存,故B错误;
C.Mg2+、NH4+、Cl-、SO42之间不发生反应,在溶液中能够大量共存,故C正确;
D.Fe3+和SCN-之间反应生成络合物,在溶液中不能大量共存,故D错误;
故选C.
点评:本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间,能发生络合反应的离子之间(如 Fe3+和 SCN-)等;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
某同学利用右图所示装置进行实验,一段时间后,水沿导管缓慢上升,下列说法正确的是( )

| A、实验过程中气球体积不会发生变化 |
| B、广口瓶内中液体的pH值增大 |
| C、广口瓶中有化合反应发生 |
| D、试管中不可能发生分解反应 |
除去铜粉中混有的少量氧化铜,其主要操作过程是( )
| A、加适量浓硫酸、微热、蒸发 |
| B、加适量稀硫酸、微热、过滤 |
| C、加适量水、微热、蒸发 |
| D、加适量稀硫酸、微热、蒸发 |
下列各组中的离子能在溶液中大量共存的是( )
| A、K+、NH4+、SO42-、OH- |
| B、Na+、Ca2+、CO32-、NO3- |
| C、Na+、H+、Cl-、HCO3- |
| D、Na+、Cu2+、Cl-、SO42- |
一定条件下,在体积一定的密闭容器中加入1mol N2和3mol H2发生反应:N2+3H22
2NH3(正反应是放热反应).下列有关说法正确的是( )
| 高温高压 |
| 催化剂 |
| A、降低温度可以加快反应速率 |
| B、达到化学反应限度时,生成2molNH3 |
| C、向容器中再加入N2,可以加快反应速率 |
| D、1mol N2和3mol H2的总能量低于2mol NH3的总能量 |
下列各分子中所有原子都满足最外层为8电子结构的是( )
| A、CH4 |
| B、NH3 |
| C、CCl4 |
| D、PCl5 |
下列有关化学方程式或离子方程式书写错误的是( )
| A、将分别蘸有浓盐酸和浓氨水的玻璃棒靠近:NH3+HCl=NH4Cl |
| B、泡沫灭火器的工作原理:3CO32-+2Al3++3H2O=2Al(OH)3↓+3CO2↑ |
| C、在酸性溶液中S2-和SO32-不能共存:2S2-+SO32-+6H+=3S↓+3H2O |
| D、不能用排空气法收集NO气体的原因:2NO+O2=2NO2 |


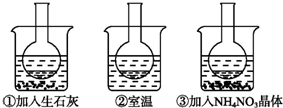 如图所示三个烧瓶中分别装入含酚酞的0.01mol?L-1 CH3COONa溶液,并分别放置在盛有水的烧杯中,然后向烧杯①中加入生石灰,烧杯②中不加任何物质,向烧杯③中加入NH4NO3晶体.
如图所示三个烧瓶中分别装入含酚酞的0.01mol?L-1 CH3COONa溶液,并分别放置在盛有水的烧杯中,然后向烧杯①中加入生石灰,烧杯②中不加任何物质,向烧杯③中加入NH4NO3晶体.