题目内容
5.0.3mol的CH4中含氢原子与10.8g水所含失误氢原子个数相等.分析 根据N=nNA可知,二者含有氢原子个数相等,说明二者含有H原子的物质的量相等,先计算出甲烷中含有H的物质的量,然后结合水的分子组成计算出水的物质的量,最后根据m=nM计算出水的质量.
解答 解:0.3mol的CH4中含有H的物质的量为:0.3mol×4=1.2mol,
二者含有H原子数相同,则含有H的物质的量相等,即水分子中含有1.2molH,则水的物质的量为:1.2mol×$\frac{1}{2}$=0.6mol,其质量为:18g/mol×0.6mol=10.8g,
故答案为:10.8.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与阿伏伽德罗常数、摩尔质量之间的关系即可解答,试题侧重基础知识的考查,有利于培养学生的化学计算能力.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
7.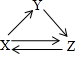 X、Y、Z三种物质存在如图所示的转化关系(图中“→”表示一步转化).下列各组物质中,不能满足此转化关系的是( )
X、Y、Z三种物质存在如图所示的转化关系(图中“→”表示一步转化).下列各组物质中,不能满足此转化关系的是( )
 X、Y、Z三种物质存在如图所示的转化关系(图中“→”表示一步转化).下列各组物质中,不能满足此转化关系的是( )
X、Y、Z三种物质存在如图所示的转化关系(图中“→”表示一步转化).下列各组物质中,不能满足此转化关系的是( )| 物质 选项 | X | Y | Z |
| A | Al | Al2O3 | Na[Al(OH)4](或NaAlO2) |
| B | Fe | FeCl3 | FeCl2 |
| C | C | CO | CO2 |
| D | Cl2 | HCl | NaCl |
| A. | A | B. | B | C. | C | D. | D |
16.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,15g甲基(-CH3)所含的中子数为6NA | |
| B. | a gO2和O3的混合气体中含有的分子总数为$\frac{a{N}_{A}}{32}$ | |
| C. | 在1L的碳酸钠溶液中,若c(CO32-)=1mol•L-1,则Na+个数为2NA | |
| D. | 78g过氧化钠晶体中,含2NA个阴离子 |
20.I6.根据下列实验操作和现象(或数据),得出的结论正确的是( )
| 操作和现象(或数据) | 结论 | |
| A | 向盛有1 mL 0.1 mol/L MgCl2溶液试管中加1 mL 0.2 mol/L NaOH溶液,有白色沉淀生成,再加入2滴0.1mol/LFeCl3溶液,又生成红褐色沉淀 | 温度相同时,Fe(OH)3溶解度小于Mg(OH)2 |
| B | 向含有少量氢氧化镁沉淀的试管中滴入NH4Cl溶液,沉淀逐渐溶解,并有刺激性的气味气体产生 | 对应的离子反应方程式为NH4++OH-═NH3↑+H2O- |
| C | 20克Ba(OH)2•8H2O粉末和10克NH4Cl粉末混合后玻璃棒迅速搅拌,可以闻到刺激性气味的气体 | 该反应为放热反应,促使氨水分解生成NH3 |
| D | 常温下,将NaAlO2溶液和NaHCO3溶液混合产生大量白色沉淀 | 说明AlO2-结合H+能力大于CO32- |
| A. | A | B. | B | C. | C | D. | D |
10.下列实验操作对应的现象与结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 常温下将铝片放入浓H2SO4中 | 生成刺激性气味气体 | Al在常温下与浓H2SO4反应生成SO2 |
| B | 向AlCl3溶液中滴加过量氨水 | 生成白色胶状物质 | Al(OH)3不溶于氨水 |
| C | 向某溶液中加入KSCN溶液,再向溶液中加入新制氯水 | 溶液先不显红色,加入氯水后变红色 | 该溶液中含有Fe3+ |
| D | 向某溶液中加入CCl4,振荡后静置 | 液体分层,下层呈紫红色 | 该溶液中含有I- |
| A. | A | B. | B | C. | C | D. | D |
14.设NA为阿伏伽德罗常数的值,下列说法中正确的是( )
| A. | 标准状况下,22.4L氧气反应时特移电子数为2NA | |
| B. | 1molCnH2n+2(n≥2)中含有的C-C键数为(n-1)NA | |
| C. | 0.1mol24Mg32S晶体中所含中子总数为28NA | |
| D. | 标准状况下,11.2LSO3所含的分子数目为0.5NA |
15.化合物F是一种医药中间体,其结构简式如图所示,下列有关F的说法正确的是( )
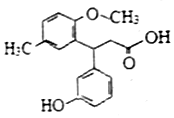

| A. | 所有碳原子可以共平面 | B. | 分子中有1个手性碳原子 | ||
| C. | 能与Na2CO3溶液反应 | D. | 能发生加成、取代、消去反应 |
 A、B、C、D、E分别是铁或铁的化合物,其中D是一种红褐色沉淀,其相互反应关系如图所示:
A、B、C、D、E分别是铁或铁的化合物,其中D是一种红褐色沉淀,其相互反应关系如图所示: