题目内容
7.下列说法正确的是( )| A. | 通过化学变化可以实现16O与18O之间的转化 | |
| B. | 因为H2O的沸点高于H2S,所以O原子得电子能力大于S原子 | |
| C. | 某化合物熔融状态下能导电,该化合物中一定有离子键 | |
| D. | 化学键是相邻分子之间的强烈的相互作用 |
分析 A.同位素之间不能通过化学反应实现转化;
B.沸点高低与原子得失电子能力无关;
C.熔融状态能导电的化合物,说明存在自由移动的离子;
D.相邻分子之间的相互作用为分子间作用力,不是化学键.
解答 解:A.16O与18O互为同位素,二者之间不能通过化学反应实现转化,故A错误;
B.水分子之间存在氢键,导致H2O的沸点高于H2S,而与O、S原子的得失电子能力无关,故B错误;
C.熔融状态能导电的化合物,说明存在自由移动的阴阳离子,离子之间通过离子键结合,则该化合物中一定有离子键,故C正确;
D.化学键是相邻的原子或离子之间强烈的相互作用,不是相邻分子之间,故D错误;
故选C.
点评 本题考查原子结构与元素性质,题目难度不大,涉及化学键、离子化合物、化学变化等知识,注意掌握化学键、化合物类型的判断方法,明确化学变化的特点,试题侧重基础知识的考查,培养了学生的分析能力及灵活应用能力.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
18.下列实验方法错误的是( )
| A. | 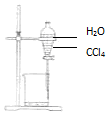 分离混合物 | B. | 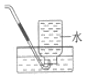 收集氨气 | C. |  保存NaOH溶液 | D. |  闻Cl2的气味 |
15.下列排列顺序正确的是( )
①热稳定性:Ca(HCO3)2>NaHCO3>CaCO3>Na2CO3
②还原性:S2->SO32->I->Fe2+>Br->Cl-
③氧化性:Fe3+>Cu2+>H+>Fe2+>Zn2+>Mg2+
④结合H+的能力:OH->AlO2->CO32->HCO3->CH3COO -
⑤酸性:H2SiO3>H2CO3>H2SO4>HClO4
⑥溶解度:CaSO4>CaCO3,Ca(NO3)2>Ca(OH)2.
①热稳定性:Ca(HCO3)2>NaHCO3>CaCO3>Na2CO3
②还原性:S2->SO32->I->Fe2+>Br->Cl-
③氧化性:Fe3+>Cu2+>H+>Fe2+>Zn2+>Mg2+
④结合H+的能力:OH->AlO2->CO32->HCO3->CH3COO -
⑤酸性:H2SiO3>H2CO3>H2SO4>HClO4
⑥溶解度:CaSO4>CaCO3,Ca(NO3)2>Ca(OH)2.
| A. | ①②③④ | B. | ①③④⑤ | C. | ②④⑤⑥ | D. | ②③④⑥ |
2.下列化学用语使用正确的是( )
| A. | 次氯酸分子的结构式:H-Cl-O | B. | 硫离子的结构示意  | ||
| C. | 质量数为37的氯原子为:37Cl | D. | 二氧化硅的分子式为:SiO2 |
12. 甲醇是重要的工业原料.煤化工可以利用煤炭制取水煤气从而合成甲醇:CO(g)+2H2(g)?CH3OH(g).
甲醇是重要的工业原料.煤化工可以利用煤炭制取水煤气从而合成甲醇:CO(g)+2H2(g)?CH3OH(g).
已知:
①图为反应的能量变化和物质键能
②CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-280kJ/mol
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-284kJ/mol
H2O(l)═H2O(g)△H=+44kJ/mol
请回答下列问题:
(1)请写出表示气态甲醇燃烧热的热化学方程式CH3OH(g)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-757kJ•mol-1.
(2)H-O键的键能x为462kJ/mol.
(3)甲醇气体分解为CO和H2两种气体的反应的活化能为510kJ/mol.
 甲醇是重要的工业原料.煤化工可以利用煤炭制取水煤气从而合成甲醇:CO(g)+2H2(g)?CH3OH(g).
甲醇是重要的工业原料.煤化工可以利用煤炭制取水煤气从而合成甲醇:CO(g)+2H2(g)?CH3OH(g).| 化学键 | H-H | H-O | O=O |
| 键能kJ/mol | 436 | x | 496 |
①图为反应的能量变化和物质键能
②CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-280kJ/mol
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-284kJ/mol
H2O(l)═H2O(g)△H=+44kJ/mol
请回答下列问题:
(1)请写出表示气态甲醇燃烧热的热化学方程式CH3OH(g)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-757kJ•mol-1.
(2)H-O键的键能x为462kJ/mol.
(3)甲醇气体分解为CO和H2两种气体的反应的活化能为510kJ/mol.
19.下列说法正确的是( )
| A. | HF、HCl、HBr、HI的熔、沸点依次升高 | |
| B. | 在NH4+和[Cu(NH3)4]2+中都存在配位键 | |
| C. | CO2、SO2都是极性分子 | |
| D. | 氯的各种含氧酸的酸性由强到弱排列为HClO>HClO2>HClO3>HClO4 |
16.下列为元素周期表中的一部分
已知:⑤的氢化物常温下为气体,该气体可使湿润的红色石蕊试纸变蓝.
用化学式或元素符号回答下列问题:
(1)④在周期表中的位置第二周期第ⅣA族.
(2)①②③中,最高价氧化物对应的水化物碱性最强的物质的电子式为 .
.
(3)①②⑥的简单离子半径由大到小的顺序是O2->Na+>Mg2+.(填离子符号)
(4)用一个化学方程式证明Cl元素与⑦非金属性的强弱:Cl2+H2S=S↓+2HCl.
(5)①和⑥形成的一种化合物A中含有一种10电子微粒和一种18电子微粒,则A中含有的化学键类型为共价键和离子键.
(6)⑥、⑦分别形成的氢化物沸点高的是H2O(填化学式).原因是H2O分子间存在氢键,氢键比分子间作用力强.
(7)①、③分别形成的最高价氧化物对应的水化物相互反应的离子方程式为OH-+Al(OH)3=AlO2-+2H2O.
| ④ | ⑤ | ⑥ | |||
| ① | ② | ③ | ⑦ |
用化学式或元素符号回答下列问题:
(1)④在周期表中的位置第二周期第ⅣA族.
(2)①②③中,最高价氧化物对应的水化物碱性最强的物质的电子式为
 .
.(3)①②⑥的简单离子半径由大到小的顺序是O2->Na+>Mg2+.(填离子符号)
(4)用一个化学方程式证明Cl元素与⑦非金属性的强弱:Cl2+H2S=S↓+2HCl.
(5)①和⑥形成的一种化合物A中含有一种10电子微粒和一种18电子微粒,则A中含有的化学键类型为共价键和离子键.
(6)⑥、⑦分别形成的氢化物沸点高的是H2O(填化学式).原因是H2O分子间存在氢键,氢键比分子间作用力强.
(7)①、③分别形成的最高价氧化物对应的水化物相互反应的离子方程式为OH-+Al(OH)3=AlO2-+2H2O.
2.取物质的量浓度为0.05mol•L-1的金属氯化物(PClx)溶液200ml,使之恰好与200ml0.15mol•L-1的AgNO3溶液完全反应.则该氯化物的化学式为( )
| A. | RCl | B. | RCl2 | C. | RCl3 | D. | RCl4 |