题目内容
19.盐酸赛庚啶是一类抗凝血、抗过敏类新药,其关键中间体H的合成路线如图: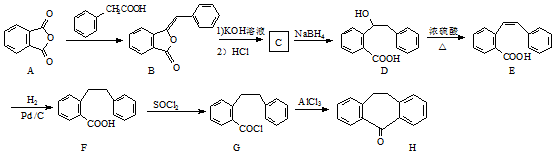
(1)D中含氧官能团名称为羟基和羧基.
(2)D→E的反应类型为消去反应.
(3)C还原可得到D,C的分子式为C15H12O3,写出C的结构简式
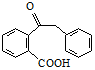 .
.(4)写出同时满足下列条件的E的一种同分异构体的结构简式
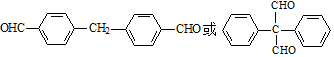 .
.①含有两个苯环且能发生银镜反应②分子中只有4种不同化学环境的氢
(5)请以
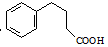 为原料制备
为原料制备 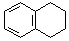 ,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干).
,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干).
分析 (1)根据D的结构简式可以判断其中含氧官能团名称;
(2)根据D→E即在浓硫酸加热条件下脱去一份子水生成双键判断;
(3)根据C还原可得到D结合C的分子式为C15H12O3,和D的结构简式判断;
(4)①含有两个苯环且能发生银镜反应,说明含有醛基;
②分子中只有4种不同化学环境的氢,说明分子结构对称性比较好;据此分析判断;
(5)根据流程中的信息F→G→H分析书写.
解答 解:(1)由D的结构简式可以判断其中含氧官能团的名称为羟基和羧基,故答案为:羟基;羧基;
(2)由流程可知D→E即在浓硫酸加热条件下脱去一份子水生成双键,所以D→E的反应类型为消去反应,故答案为:消去反应;
(3)C还原可得到D,由D的结构式推出D的分子式为C15H14O3,又C的分子式为C15H12O3,所以C→D即增加2个H,则C的结构简式 ,故答案为:
,故答案为: ;
;
(4)①含有两个苯环且能发生银镜反应,说明含有醛基;②分子中只有4种不同化学环境的氢,说明分子结构对称性比较好,又除了2个苯环外,有2个O,2个不饱和度,所以应该为对称的2个醛基,则符合条件的同分异构体为 ;故答案为:
;故答案为:
(5)由流程中的信息F→G→H,则可以将羧基变成羰基,再根据C→D将羰基还原成羟基,后根据D→E→F经过消去加成去掉羟基即可,则流程图为: ,故答案为:
,故答案为: .
.
点评 本题考查有机物的推断与合成、官能团结构与性质、性质条件同分异构体书写等,注意掌握有机物官能团的性质和转化,结合反应条件与有机物结构进行分析,难度中等.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
9.对于已达到平衡的可逆反应:A(g)?2B(?)+C(g)△H>0,假设A、C状态保持不变,下列说法正确的是( )
| A. | 当混合气体的质量不变,说明反应已达平衡状态 | |
| B. | 缩小容器体积,重新达到平衡时,气体混合物中C%可能增大 | |
| C. | 在恒压容器中升高温度,气体混合物中C%可能先增大后减小 | |
| D. | 在恒容容器中升高温度,达到新平衡时,气体的密度增大 |
10.氨碱法(索氏)和联合制碱法(侯氏)是两大重要的工业制碱法,下列表达正确的是( )
| 氨碱法 | 联合制碱法 | ||
| A. | 原料 | 食盐、氨气、生石灰 | 食盐、氨气、二氧化碳 |
| B. | 副产物 | 氯化钙 | 氯化铵 |
| C. | 循环物质 | 氨气、二氧化碳 | 氯化钠 |
| D. | 评价 | 原料易得;设备复杂;能耗高 | 原料利用率高;废弃物少 |
| A. | A | B. | B | C. | C | D. | D |
7.某可逆反应:A(g)+3B(g)?2C(g);△H<0.有甲乙两个容积为0.5L的密闭容器,向甲容器中加入1molA的和3molB在一定条件下达到平衡时放出热量为Q1kJ;在相同条件下,向乙容器中加入2molC达到平衡时吸收热量为Q2kJ;已知Q2=3Q1.下列叙述正确的是( )
| A. | 乙中的热化学方程式为2C(g)?A(g)+3B(g);△H=+4Q2/3kJ/mol | |
| B. | 反应达到平衡前,甲中始终有v正大于v逆,乙中始终有v正大于v逆 | |
| C. | 在该条件下,反应2C(g)?A(g)+3B(g)的平衡常数为9×1.52(mol/L)2 | |
| D. | 乙中C的转化率为25% |
14.下列氯化物不能用金属与盐酸反应得到的是( )
①FeCl3 ②FeCl2③CuCl2 ④MgCl2.
①FeCl3 ②FeCl2③CuCl2 ④MgCl2.
| A. | ①②③ | B. | ①③ | C. | ②④ | D. | ①④ |
4.下列反应的离子方程式书写正确的是( )
| A. | 碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ | |
| B. | 稀H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 氢氧化钡溶液与稀H2SO4反应:Ba2++SO42-=BaSO4↓ | |
| D. | 将氢氧化铁放入盐酸中:Fe(OH)3+3H+=Fe3++3H2O |
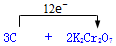 .
.