题目内容
有A、B、C、D、E、F六种元素,其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数;B原子最外层中有两个不成对的电子;D、E原子核内各自的质子数与中子数相等;B元素可分别与A、C、D、E生成RB2型化合物,并知在DB2和EB2中,D与B的质量比为7:8;E与B的质量比为1:1.F+离子的3d轨道中电子全充满.回答下列问题:
(1)写出基态E原子的电子排布式 .
(2)用电子式表示AE2的形成过程 .
(3)B、C两元素的第一电离能大小关系为: > (填写元素符号),原因是 .
(4)B元素的最低价氢化物分子立体构型为 .中心原子的杂化方式为 .
(5)向F2+离子的溶液中加入过量CH3的浓溶液,充分反应后溶液呈深蓝色,该反应的离子方程式是 .
(1)写出基态E原子的电子排布式
(2)用电子式表示AE2的形成过程
(3)B、C两元素的第一电离能大小关系为:
(4)B元素的最低价氢化物分子立体构型为
(5)向F2+离子的溶液中加入过量CH3的浓溶液,充分反应后溶液呈深蓝色,该反应的离子方程式是
考点:位置结构性质的相互关系应用
专题:
分析:p能级电子数不超过6,A原子最外层p能级的电子数等于次外层的电子数总数,则A的核外电子排布为1s22s22p2,应为C元素,B原子最外层中有两个不成对的电子,核外电子排布式为1s22s22p4,为O元素,B元素可分别与A、C、D、E生成RB2型化合物,且A、B、C属于同一周期,则C为N元素,可形成NO2化合物,在DB2和EB2中,D与B的质量比为7:8,则有M(D):M(O)=7:4,M(D)=7×
=28,D应为Si元素;E与B的质量比为1:1,则M(E)=2M(O)=2×16=32,所以E为S元素,F+离子的3d轨道中电子全充满,则F为Cu.结合元素对应原子的结构、单质以及化合物的性质解答该题.
| 16 |
| 4 |
解答:
解:p能级电子数不超过6,A原子最外层p能级的电子数等于次外层的电子数总数,则A的核外电子排布为1s22s22p2,应为C元素,B原子最外层中有两个不成对的电子,核外电子排布式为1s22s22p4,为O元素,B元素可分别与A、C、D、E生成RB2型化合物,且A、B、C属于同一周期,则C为N元素,可形成NO2化合物,在DB2和EB2中,D与B的质量比为7:8,则有M(D):M(O)=7:4,M(D)=7×
=28,D应为Si元素;E与B的质量比为1:1,则M(E)=2M(O)=2×16=32,所以E为S元素,F+离子的3d轨道中电子全充满,则F为Cu.
(1)E为S元素,原子序数为16,基态原子的核外电子排布式为1s22s22p63s23p4,
故答案为:1s22s22p63s23p4;
(2)AE2为CS2,为共价化合物,根据化合物中各原子最外层满足8电子稳定结构,可写出用电子式表示的形成过程为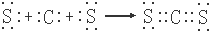 ,
,
故答案为: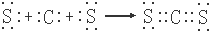 ;
;
(3)由于N原子2p轨道为半充满状态,第一电离能较大,所以第一电离能N>O,故答案为:N,O;N原子中最外层电子处于半充满状态,比较稳定,
(4)H2O中,O原子与H原子形成2个δ键,孤电子对数为
=2,空间构型为V形,O原子的杂化轨道类型为sp3杂化,
故答案为:V形;sp3;
(5)向Cu2+离子的溶液中加入过量NH3的浓溶液,充分反应后溶液呈深蓝色,生成四氨合铜离子,离子方程:Cu2++4NH3?H2O=[Cu(NH3)4]2++4H2O,
故答案为:Cu2++4NH3?H2O=[Cu(NH3)4]2++4H2O.
| 16 |
| 4 |
(1)E为S元素,原子序数为16,基态原子的核外电子排布式为1s22s22p63s23p4,
故答案为:1s22s22p63s23p4;
(2)AE2为CS2,为共价化合物,根据化合物中各原子最外层满足8电子稳定结构,可写出用电子式表示的形成过程为
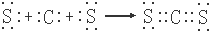 ,
,故答案为:
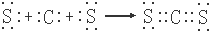 ;
;(3)由于N原子2p轨道为半充满状态,第一电离能较大,所以第一电离能N>O,故答案为:N,O;N原子中最外层电子处于半充满状态,比较稳定,
(4)H2O中,O原子与H原子形成2个δ键,孤电子对数为
| 6-2×1 |
| 2 |
故答案为:V形;sp3;
(5)向Cu2+离子的溶液中加入过量NH3的浓溶液,充分反应后溶液呈深蓝色,生成四氨合铜离子,离子方程:Cu2++4NH3?H2O=[Cu(NH3)4]2++4H2O,
故答案为:Cu2++4NH3?H2O=[Cu(NH3)4]2++4H2O.
点评:本题考查较为综合,涉及元素的推断、电子排布式的书写、电子式、第一电离能、杂化类型以及元素周期律等知识,题目难度中等,本题中正确推断元素的种类为解答该题的关键.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
下列反应中,离子方程式正确的是( )
| A、铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
| B、碳酸钙跟盐酸反应:CO32-+2H+=H2O+CO2↑ |
| C、稀硫酸跟氢氧化钾溶液反应:H++OH-═H2O |
| D、氢氧化钡溶液跟稀硫酸反应:Ba2++SO42-═BaSO4↓ |
下列化学用语中,书写正确的是( )
| A、乙烯的结构简式:CH2CH2 |
| B、水的结构式:H-O-H |
C、氨分子的电子式: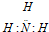 |
D、硫原子的结构示意图: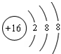 |
下列物质中不能发生水解反应的是( )
| A、蛋白质 | B、淀粉 |
| C、葡萄糖 | D、脂肪 |