题目内容
(18分)(1)若NA为阿伏伽德罗常数,则3.4g氨气中所含氢原子个数为 。
(2)约3.01×1023个OH-的质量为 g,含有电子的物质的量为 ,这些OH-与 mol NH3的质量相同。
(3)将4gNaOH固体溶于水配成250mL溶液,此溶液中NaOH的物质的量浓度为 __mol/L。取出10mL溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为_____________mol/L。
(4)现有M、N两种气态化合物,其摩尔质量之比为2:1,试回答下列问题:
①同温同压下,M、N气体的密度之比为____________
②相同温度下,在两个相同体积的密闭容器中分别充入M、N,若两个容器中气体的密度相等,则两个容器中的压强之比为____________
③将M、N两种气体分别溶于水(M、N与水均不反应)配成溶液,当两种溶液的质量分数相同时,其密度分别为d1和d2,则两种溶液的物质的量浓度之比为____________。
25、(1)0.6NA (2)8.5g;5mol;0.5 (3) 0.4; 0.04 (4) ①2:1 ②1:2 ③d1:2d2
【解析】
试题分析:(1)氨气的相对分子质量是17,其摩尔质量是17g/mol,则3.4g氨气的物质的量为:n(NH3)=3.4/17=0.2mol,所以含有氨气的分子数为:N(NH3)=nNA=0.2×NA=0.2NA;含有氢原子的数目为:N(H)=3N(NH3)=0.6NA,(2)约3.01×1023个OH-的物质的量为0.5mol,0.5mol氢氧根离子的质量为:17g/mol×0.5mol=8.5g;0.5mol氢氧根离子含有电子的物质的量为:0.5mol×10=5mol;含有5mol电子,需要氨气的物质的量为:5/10=0.5mol,答案为:8.5g;5mol;0.5;(3) (3)将4gNaOH固体溶于水制成250ml溶液,溶质氢氧化钠物质的量n=4/40=0.1mol,氢氧化钠溶液的物质的量浓度c=0.1/0.25=0.4mol/L,取出10ml此溶液,溶质浓度不变为0.4mol/L,将取出的10mL溶液加水稀释到100ml,依据稀释前后溶质物质的量不变,稀释后溶液中NaOH的物质的量浓度为c,得到:0.01L×0.4mol/L=0.1L×c,得到:c=0.04mol/L,答案为:0.4; 0.04;(4)①相同条件下,M、N气体的密度之比与其摩尔质量成正比,所以二者的密度之比为:2:1,答案为:2:1;②两个容器中气体的密度相同,则气体的质量相等,物质的量与摩尔质量成反比,而压强与气体的物质的量成正比,则容器中气体的压强与摩尔质量成反比,两个容器中压强之比为:1:2答案为:1:2;③两种溶液的质量分数相同时,由c=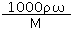 可知,溶液的物质的量浓度与
可知,溶液的物质的量浓度与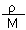 成正比,所以两种溶液的物质的量浓度之比为:
成正比,所以两种溶液的物质的量浓度之比为: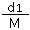 :
: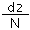 =d1:2 d2,答案为:d1:2 d2.
=d1:2 d2,答案为:d1:2 d2.
考点:考查阿伏伽德罗常数、物质的量浓度的计算等知识。




 +H++H2O===Al(OH)3↓
+H++H2O===Al(OH)3↓ 与
与