题目内容
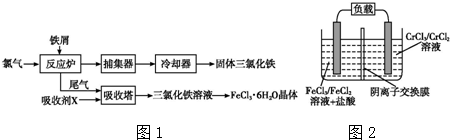
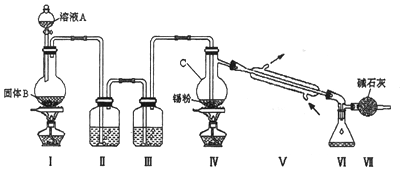
14.四氯化锡用作媒染剂和有机合成的氯化催化剂,实验室制备四氯化锡的反应、装置示意图和有关信息如下: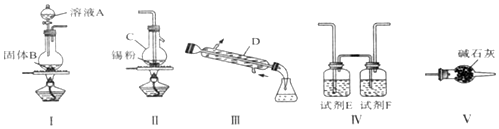
有关信息:
①将金属锡熔融,通入干燥氯气进行反应,生成四氯化锡.
②无水四氯化锡是无色易流动的液体,熔点-33℃,沸点114.1℃.
⑧暴露于空气中与空气中的水分反应生成白烟,有强烈的刺激性,遇水分解.
回答下列问题:
(1)仪器C的名称是蒸馏烧瓶.
(2)制备无水四氯化锡各装置的连接顺序是Ⅰ→Ⅳ→Ⅱ→Ⅲ→Ⅴ(填装置序号).
(3)装置V的作用是吸收未反应完全的氯气,防止空气中的水气进入装置Ⅲ内,使SnCl4水解.
(4)若无装置V存在,在装置Ⅲ中除生成SnCl4外,还存在的副产物化学式为Sn(OH)4或SnO2.
(5)若Ⅱ中用去锡粉5.95g,反应后,Ⅲ中锥形瓶里收集到12.0g SnCl4,则SnCl4的产率为92.0%.
分析 由装置图可知装置Ⅰ应为制备氯气装置,离子反应为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,装置E为饱和食盐水,装置F为浓硫酸,氯气经除杂,干燥后与锡在装置Ⅱ中反应生成SnCl4,经冷却后在装置Ⅲ中收集,因SnCl4极易水解,应防止空气中的水蒸气进入装置Ⅲ中,通过连接装置V来实现,
(1)仪器图形和作用可知为蒸馏烧瓶;
(2)该实验中先制备氯气,氯气经除杂,干燥后与锡在装置Ⅱ中反应生成SnCl4,经冷却后在装置Ⅲ中收集,因SnCl4极易水解,应防止空气中的水蒸气进入装置Ⅲ中;
(3)碱石灰可以吸收空气中水蒸气防止空气中的水蒸气进入装置E中,使SnCl4水解;
(4)若无装置V存在,则在氯气中含有水蒸汽,SnCl4水解产生的含锡的化合物;
(5)若Ⅱ中用去锡粉5.95g,则n(Sn)=$\frac{5.95g}{119g/mol}$=0.05mol,理论上产生的SnCl4的物质的质量是m(SnCl4)=0.05mol×261g/mol=13.05g,产率=$\frac{实际产量}{理论产量}$×100%;
解答 解:(1)由装置图可知仪器C为蒸馏烧瓶,故答案为:蒸馏烧瓶;
(2)该实验中先制备氯气,氯气经除杂,干燥后与锡在装置Ⅱ中反应生成SnCl4,经冷却后在装置Ⅲ中收集,因SnCl4极易水解,应防止空气中的水蒸气进入装置Ⅲ中,所以连接顺序是I→Ⅳ→Ⅱ→Ⅲ→V;
故答案为:I;Ⅳ;Ⅱ;Ⅲ;V;
(3)装置Ⅰ中这制得的氯气中含有氯化氢和水蒸气,装置E为饱和食盐水,除去氯化氢,装置F为浓硫酸,除去水蒸气;因SnCl4极易水解,应防止空气中的水蒸气进入装置Ⅲ中,通过连接装置V来实现;
故答案为:吸收未反应的氯气;防止空气中的水蒸气进入装置Ⅲ内,使SnCl4水解;
(4)若无装置V存在,则在氯气中含有水蒸汽,所以在Ⅲ中除生成SnCl4外,还会生成SnCl4水解产生的含锡的化合物Sn(OH)4或SnO2;
故答案为:Sn(OH)4或SnO2;
(5)若Ⅱ中用去锡粉5.95g,则n(Sn)=$\frac{5.95g}{119g/mol}$=0.05mol,理论上产生的SnCl4的物质的质量是m(SnCl4)=0.05mol×261g/mol=13.05g,所以反应后,Ⅲ中锥形瓶里收集到12.0gSnCl4,则SnCl4的产率为$\frac{12.0g}{13.05g}$×100%=92.0%,
故答案为:92.0%.
点评 本题考查物质的制备,涉及仪器的识别、氯气的实验室制取方法、实验操作的目的、盐类水解、物质产率的计算等知识,侧重于学生的分析能力、实验能力的考查,注意把握题给信息,结合物质的性质设计实验步骤,题目难度中等.

| 密度/(g•cm-3) | 沸点/℃ | 水溶性 | |
| 1-丁醇 | 0.81 | 117.7 | 可溶 |
| 乙 酸 | 1.05 | 117.9 | 互溶 |
| 乙酸丁酯 | 0.88 | 126.3 | 微溶 |
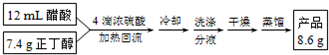
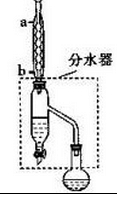
(1)装置a的名称是球形冷凝管,其中冷却水的流动方向是下口进上口出.
(2)制取乙酸丁酯的化学方程式为CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH2CH2CH3+H2O.加热回流时,分水器中液体分为两层,适时放出水使上层液体流入烧瓶b,从平衡角度考虑,分水器的作用是除去酯化反应生成的水,使生成乙酸丁酯的平衡向正反应方向移动.
(3)反应结束后,把分水器中的酯层和b中的反应液一起倒入分液漏斗中.在分液漏斗中加入10 mL水洗涤,除去下层,上层继续用10 mL 10% Na2CO3溶液洗涤至中性,分液后将上层液体再用10 mL水洗涤,除去溶于酯中的少量无机盐.下列说法不正确的是D(填序号).
A.最初用10 mL水洗涤的目的是除去酸及少量的正丁醇
B.用10 mL 10% Na2CO3洗涤的目的是除去残留的硫酸和乙酸
C.分液时先将水层从分液漏斗的下口放出,再将乙酸丁酯从上口到出
D.分液时先将水层从分液漏斗的下口放出,再将乙酸丁酯从下口放出
(4)在洗涤、分液后的乙酸丁酯中加入少量无水硫酸镁,其目的是除去乙酸丁酯中的水(或干燥乙酸丁酯).
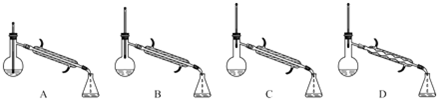
(5)在蒸馏操作中,仪器选择及安装都正确的是C(填标号).
(6)本实验的产率是74%.
| A. | 物质发生化学变化不一定伴随着能量变化 | |
| B. | 硫酸钡、醋酸铵、氨水都是弱电解质 | |
| C. | 向0.1 mol•L-1 Na2CO3溶液中滴加酚酞,溶液变红色 | |
| D. | 在温度、压强一定的条件下,自发反应总是向△H-T△S<0的方向进行 |
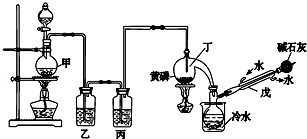
有关物质的部分性质如下:
| 熔点/℃ | 沸点/℃ | 其他 | |
| 黄磷 | 44.1 | 280.5 | 2P(过量)+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2PCl3;2P+5Cl2(过量)$\frac{\underline{\;\;△\;\;}}{\;}$2PCl5 |
| PCl3 | -112 | 75.5 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
| POCl3 | 2 | 105.3 | 遇水生成H3PO4和HCl,能溶于PCl3 |
(1)仪器戊的名称为冷凝管.
(2)实验时甲中所发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(3)乙中盛放的试剂是饱和氯化钠溶液,其作用是除去氯气中的氯化氢;丙中盛放的试剂是浓硫酸,其作用是除去氯气中的水蒸气.
(4)向仪器丁中通入干燥、纯净的Cl2之前,应先通入一段时间的CO2,其目的主要是排净装置中的空气,防止空气中的水分和氧气与PCl3反应
(5)碱石灰的作用是碱石灰吸收多余氯气防止污染空气,防止空气中的水蒸气进入影响产品纯度(答出一条即可).
(6)PCl3粗产品中常含有POCl3、PCl5等,加入黄磷(化学式用P表示)经加热除去PCl5的化学反应方程式为3PCl5+2P$\frac{\underline{\;\;△\;\;}}{\;}$5PCl3,后通过蒸馏(填实验操作名称),即可得到PCl3纯品.
①混合气体的压强 ②混合气体的密度
③B的物质的量浓度 ④混合气体总物质的量
⑤混合气体的平均相对分子质量 ⑥v(C)与v(D)的比值 ⑦混合气体总质量.
| A. | ①②③④⑤⑥⑦ | B. | ①⑤ | C. | ②⑤⑦ | D. | ①③④⑤ |
| A. | 明朝的《本草纲目》记载“烧酒非古法也,自元时创始,其法用浓酒和糟入甑(指蒸锅),蒸令气上,用器承滴露.”该段文字记载了白酒(烧酒)的制造过程中采用了蒸馏的方法来分离和提纯 | |
| B. | 汉朝的《淮南万毕术》、《神农本草经》记载“白青(碱式碳酸铜)得铁化为铜”,“石胆…能化铁为铜”都是指铜可以采用湿法冶炼 | |
| C. | 清初《泉州府志》物产条载:“初,人不知盖泥法,元时南安有黄长者为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之.”该段文字记载了蔗糖的分离提纯采用了黄泥来吸附红糖中的色素 | |
| D. | 晋代葛洪的《抱朴子》记载“丹砂烧之成水银,积变又成丹砂”,是指加热时丹砂(HgS)熔融成液态,冷却时重新结晶为HgS晶体 |