题目内容
现有物质A~I,其转化关系如下图,已知:A为两种元素组成的化合物,B不溶于水,X常温下为无色液体,E常温下为红棕色气体.(反应中生成的其它物质已略去)

根据上述转化关系图回答:
(1)写出下列物质的化学式X ;J
(2)物质H的电子式:
物质J是属于哪种晶体类型:
(3)按要求写出下列方程式
写出反应①的化学方程式 ;
写出反应③的化学方程式 ;
写出反应②的离子方程式 .

根据上述转化关系图回答:
(1)写出下列物质的化学式X
(2)物质H的电子式:
物质J是属于哪种晶体类型:
(3)按要求写出下列方程式
写出反应①的化学方程式
写出反应③的化学方程式
写出反应②的离子方程式
考点:无机物的推断
专题:推断题
分析:X常温下为无色液体,应为H2O,A为两种元素组成的化合物,和水反应生成B既能与盐酸反应又能与氢氧化钠反应,应为Al(OH)3,E常温下为红棕色气体,应为NO2,则D为NO,Y为O2,H为NH3,A为AlN,I为HNO3,J为NH4NO3,结合对应物质的性子以及题目要求解答该题.
解答:
解:X常温下为无色液体,应为H2O,A为两种元素组成的化合物,和水反应生成B既能与盐酸反应又能与氢氧化钠反应,应为Al(OH)3,E常温下为红棕色气体,应为NO2,则D为NO,Y为O2,H为NH3,A为AlN,I为HNO3,J为NH4NO3,
(1)由以上分析可知X为H2O,J为NH4NO3,故答案为:H2O; NH4NO3;
(2)H为NH3,电子式为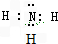 ,J为NH4NO3,为离子晶体,故答案为:
,J为NH4NO3,为离子晶体,故答案为: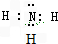 ; 离子晶体;
; 离子晶体;
(3)反应①为AlN的水解,生成氢氧化铝和氨气,反应的化学方程式为AlN+3H2O=Al(OH)3+NH3,反应③为氨气的催化氧化,方程式为4NH3+5O2
4NO+6H2O,
反应②为氢氧化铝与氢氧化钠的反应,反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,
故答案为:AlN+3H2O=Al(OH)3+NH3; 4NH3+5O2
4NO+6H2O;Al(OH)3+OH-=AlO2-+2H2O.
(1)由以上分析可知X为H2O,J为NH4NO3,故答案为:H2O; NH4NO3;
(2)H为NH3,电子式为
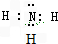 ,J为NH4NO3,为离子晶体,故答案为:
,J为NH4NO3,为离子晶体,故答案为: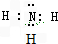 ; 离子晶体;
; 离子晶体;(3)反应①为AlN的水解,生成氢氧化铝和氨气,反应的化学方程式为AlN+3H2O=Al(OH)3+NH3,反应③为氨气的催化氧化,方程式为4NH3+5O2
| ||
| 高温高压 |
反应②为氢氧化铝与氢氧化钠的反应,反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,
故答案为:AlN+3H2O=Al(OH)3+NH3; 4NH3+5O2
| ||
| 高温高压 |
点评:本题考查元素化合物的推断,为高考常见题型,侧重于学生的分析能力的考查,做题注意抓住题目中的颜色、状态等关键信心作为做题的突破口,本题较为综合,具有一定难度.

练习册系列答案
相关题目
下列反应的离子方程式书写正确的是( )
| A、盐酸滴入氨水中:H++OH-=H2O |
| B、Na2S的水解反应:S2-+2H2O=H2S↑+2OH- |
| C、在碳酸氢镁溶液中加入足量Ca(OH)2溶液:Mg2++2HCO3-+Ca2++2OH一=MgCO3↓+CaCO3↓+2H2O |
| D、铜片插入硝酸银溶液中:Cu+2Ag+=Cu2++2Ag |
下列有关化学用语表示正确的是( )
| A、乙烯的结构简式:C2H4 | ||
B、中子数为20的钾原子:
| ||
C、次氯酸的电子式: | ||
D、CH4分子的比例模型: |
 如图表示25℃时,0.1mol/L的一元弱酸HA加水稀释过程中,某量随加水量变化情况,则图中纵坐标y可以是( )
如图表示25℃时,0.1mol/L的一元弱酸HA加水稀释过程中,某量随加水量变化情况,则图中纵坐标y可以是( )| A、溶液的pH | ||
| B、Ka(HA) | ||
C、
| ||
D、
|
已知热化学方程式C2H2(g)+
O2(g)=2CO2(g)+H2O(g)△H=-1256kJ/mol,下列说法正确的是( )
| 5 |
| 2 |
| A、乙炔的燃烧热为1256 kJ/mol |
| B、若转移10 mol电子,则消耗2.5 mol O2 |
| C、该反应在给定条件下是一个熵增焓减的反应 |
| D、若形成4 mol碳氧共用电子对,则放出的热量为2512 kJ |
 一定条件下,Cu2+、Mn2+、Fe3+的浓度对乙酸在光照下催化降解速率的影响如图所示.下列判断不正确的是( )
一定条件下,Cu2+、Mn2+、Fe3+的浓度对乙酸在光照下催化降解速率的影响如图所示.下列判断不正确的是( )| A、Cu2+、Mn2+提高乙酸降解速率的最佳浓度为0.1 mol?L-l |
| B、Fe3+不能提高乙酸降解速率 |
| C、相同条件下,乙酸在Cu2+、Mn2+、Fe3+作用下的降解速率依次减小 |
| D、该实验方案的缺陷之一是未做空白对照实验 |

