题目内容
17.下列离子方程式,一定不正确的是.( )| A. | 实验室用石灰石和盐酸反应制取CO2:CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | H2O2溶液中滴加酸性KMnO4溶液:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O | |
| C. | 铁屑溶于过量稀硝酸:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| D. | NaHCO3溶液与足量Ba(OH)2溶液反应:HCO3-+Ba2++OH-═BaCO3↓+H2O |
分析 A.反应生成氯化钙、水、二氧化碳;
B.发生氧化还原反应,遵循电子、电荷守恒;
C.反应生成硝酸铁、NO和水;
D.碳酸氢钠完全反应,生成碳酸钡、水、NaOH.
解答 解:A.实验室用石灰石和盐酸反应制取CO2的离子反应为CaCO3+2H+═Ca2++CO2↑+H2O,故A正确;
B.H2O2溶液中滴加酸性KMnO4溶液的离子反应为2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O,故B正确;
C.铁屑溶于过量稀硝酸的离子反应为Fe+4H++NO3-═Fe3++NO↑+2H2O,故C错误;
D.NaHCO3溶液与足量Ba(OH)2溶液反应的离子反应为HCO3-+Ba2++OH-═BaCO3↓+H2O,故D正确;
故选C.
点评 本题考查离子反应书写的正误判断,为高频考点,把握常见离子之间的反应为解答的关键,侧重氧化还原反应、复分解反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
7.NA为阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 常温下,23 g NO2和N2O4的混合气体中含有NA个氧原子 | |
| B. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为1 NA | |
| C. | 7.1gCl2与足量的氢氧化钠溶液反应转移的电子数为0.2NA | |
| D. | 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |
12.现有下列四个图象:

下列反应中全部符合上述图象的反应是( )

下列反应中全部符合上述图象的反应是( )
| A. | N2(g)+3H2(g)?2NH3(g);△H=-Q1kJ/mol(Q1>0) | |
| B. | 2SO3(g)?2SO2(g)+O2(g);△H=+Q2 kJ/mol(Q2>0) | |
| C. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g);△H=-808.7 kJ/mol | |
| D. | 2CO(g)?C(s)+CO2(g);△H=-171.4kJ/mol |
2.将煤粉隔绝空气加强热,除主要得到焦炭外,还能得到下表所列的物质:
(1)表中所列物质不属于有机物的是(填序号):②⑦.
(2)能与溴水反应使之褪色的烃是(填序号):③⑥⑦.
(3)彼此互为同系物的是(填序号):④⑤.
(4)能发生加聚反应、生成物可用作制造食品包装袋的是(填序号)③,该物质发生加聚反应的化学方程式为: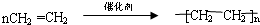 .
.
(5)甲苯的一氯取代产物有4种.
| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 名称 | 甲烷 | 一氧化碳 | 乙烯 | 苯 | 甲苯 | 苯酚 | 氨水 |
(2)能与溴水反应使之褪色的烃是(填序号):③⑥⑦.
(3)彼此互为同系物的是(填序号):④⑤.
(4)能发生加聚反应、生成物可用作制造食品包装袋的是(填序号)③,该物质发生加聚反应的化学方程式为:
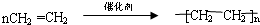 .
.(5)甲苯的一氯取代产物有4种.
6.某烃的结构简式为 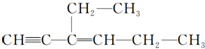 分子中处于四面体结构中心的碳原子数为a,一定处在同一平面内的碳原子数为b,一定处在同一直线上的碳原子数为c,则a、b、c依次为( )
分子中处于四面体结构中心的碳原子数为a,一定处在同一平面内的碳原子数为b,一定处在同一直线上的碳原子数为c,则a、b、c依次为( )
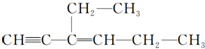 分子中处于四面体结构中心的碳原子数为a,一定处在同一平面内的碳原子数为b,一定处在同一直线上的碳原子数为c,则a、b、c依次为( )
分子中处于四面体结构中心的碳原子数为a,一定处在同一平面内的碳原子数为b,一定处在同一直线上的碳原子数为c,则a、b、c依次为( )| A. | 4、5、3 | B. | 4、6、3 | C. | 2、4、5 | D. | 4、4、6 |
7.向含有下列微粒的溶液中分别加入少量NaOH固体、少量浓盐酸或少量高锰酸钾溶液,都能使该微粒浓度下降的是( )
| A. | Fe3+ | B. | HS- | C. | HCO3- | D. | C6H5O- |