题目内容
(1)写出一氧化碳还原氧化铁的化学方程式 ,氧化剂为
(2)镁在二氧化碳中的燃烧的化学方程式:
(3)写出氧化铜溶解于稀硫酸的离子反应方程式:
(4)工业制漂白粉的化学方程式: .
(2)镁在二氧化碳中的燃烧的化学方程式:
(3)写出氧化铜溶解于稀硫酸的离子反应方程式:
(4)工业制漂白粉的化学方程式:
考点:化学方程式的书写
专题:元素及其化合物
分析:(1)一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,氧化剂为氧化铁;
(2)镁条在二氧化碳中燃烧生成氧化镁和黑色粉末;
(3)氧化铜为碱性氧化物和稀硫酸反应生成硫酸铜和水,据此写出反应的离子方程式;
(4)工业上将Cl2通入石灰乳制取漂白粉,产物为CaCl2和Ca(ClO)2和水,漂白粉的成分是CaCl2和Ca(ClO)2的混合物.
(2)镁条在二氧化碳中燃烧生成氧化镁和黑色粉末;
(3)氧化铜为碱性氧化物和稀硫酸反应生成硫酸铜和水,据此写出反应的离子方程式;
(4)工业上将Cl2通入石灰乳制取漂白粉,产物为CaCl2和Ca(ClO)2和水,漂白粉的成分是CaCl2和Ca(ClO)2的混合物.
解答:
解:(1)一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO
2Fe+3CO2,氧化剂为Fe2O3,
故答案为:Fe2O3+3CO
2Fe+3CO2;Fe2O3;
(2)镁条在二氧化碳中燃烧生成氧化镁和黑色粉末,反应的化学方程式为:2Mg+CO2
2MgO+C,
故答案为:2Mg+CO2
2MgO+C;
(3)氧化铜溶解于稀硫酸,氧化铜为碱性氧化物和稀硫酸反应生成硫酸铜和水,反应的化学反应方程式为:CuO+H2SO4=CuSO4+H2O,根据离子方程式的书写原则可得该反应的离子方程式为:CuO+2H+=Cu2++H2O,
故答案为:CuO+2H+=Cu2++H2O;
(4)工业上用氯气和熟石灰来制取漂白粉,原理是:Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,
故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
| ||
故答案为:Fe2O3+3CO
| ||
(2)镁条在二氧化碳中燃烧生成氧化镁和黑色粉末,反应的化学方程式为:2Mg+CO2
| ||
故答案为:2Mg+CO2
| ||
(3)氧化铜溶解于稀硫酸,氧化铜为碱性氧化物和稀硫酸反应生成硫酸铜和水,反应的化学反应方程式为:CuO+H2SO4=CuSO4+H2O,根据离子方程式的书写原则可得该反应的离子方程式为:CuO+2H+=Cu2++H2O,
故答案为:CuO+2H+=Cu2++H2O;
(4)工业上用氯气和熟石灰来制取漂白粉,原理是:Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,
故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
点评:本题考查学生根据反应原理书写方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等,注意根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写,题目难度不大.

练习册系列答案
相关题目
下列叙述中不正确的是( )
| A、除去FeCl2溶液中的FeCl3杂质,可以向溶液中加入过量铁粉,然后过滤 |
| B、Na2O2用于呼吸面具,活性炭用于防毒面具,两者原理不同 |
| C、NaOH、Na2CO3、NaHCO3的溶液均呈碱性,所以可以共存 |
| D、62g Na2O和78g Na2O2分别溶于等量且足量的水中,所得溶液中溶质的质量分数相等 |
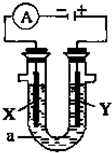 (1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是



