题目内容
3.Cl2和SO2都具有漂白作用,能使品红溶液褪色.若将等物质的量的Cl2、SO2混合后,再通入品红溶液与BaCl2的混合溶液,能观察到的现象是( )| A. | 溶液很快褪色 | B. | 溶液不褪色 | C. | 出现沉淀 | D. | 不出现沉淀 |
分析 将等物质的量的SO2和Cl2反应生成盐酸和硫酸,再通入品红与BaCl2的混合溶液,依据生成盐酸和硫酸的性质判断发生反应及现象,硫酸和氯化钡反应会出现白色沉淀,据此解答.
解答 解:等物质的量的SO2和Cl2混合后的气体溶解于适量的蒸馏水中,发生反应:SO2+Cl2+2H2O=2HCl+H2SO4,生成盐酸和硫酸都不具有漂白性,所以不能使品红溶液,硫酸与氯化钡反应生成硫酸钡沉淀,H2SO4+BaCl2=BaSO4↓+2HCl,所以会产生白色沉淀,
故选BC.
点评 本题考查氯气和二氧化硫的反应,明确二者发生反应及生成物的性质是解题关键,题目难度不大.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
11.下列电离方程式正确的是( )
| A. | Na2CO3→Na++CO32- | B. | H2S→2H++S2- | ||
| C. | H2CO3→H++HCO3- | D. | NaHSO4→Na++H++SO42- |
15.以下能级符号不正确的是( )
| A. | 6s | B. | 2d | C. | 3p | D. | 7f |
12.某有机物的结构简式如图所示,下列有关该有机物的说法中正确的是( )
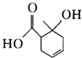

| A. | 能和碳酸钠溶液反应的官能团有2种 | |
| B. | 1mol该有机物最多能与2molH2发生加成 | |
| C. | 与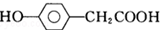 互为同分异构体 互为同分异构体 | |
| D. | 既可以发生取代反应又可以发生氧化反应 |
13.区别硫酸铜溶液和氢氧化铁胶体最简单的方法是( )
| A. | 丁达尔效应 | B. | 观察溶液颜色 | C. | 过滤 | D. | 加热 |
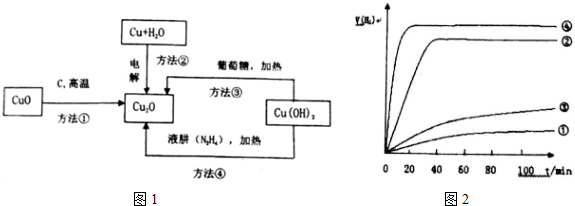
 (制酚醛树脂)④
(制酚醛树脂)④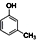 (生产杀虫剂)⑤CH2=CH─CH=CH2(合成橡胶原料)⑥HCHO(防腐剂)
(生产杀虫剂)⑤CH2=CH─CH=CH2(合成橡胶原料)⑥HCHO(防腐剂)