题目内容
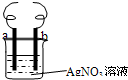 用铜丝(电极a)、银丝(电极b)和AgNO3溶液可以构成原电池或电解池,如图.则下列说法正确的是( )
用铜丝(电极a)、银丝(电极b)和AgNO3溶液可以构成原电池或电解池,如图.则下列说法正确的是( )| A、构成原电池时b极反应为:Cu2++2e-=Cu |
| B、构成电解池时a极质量一定减少 |
| C、构成电解池时b极质量可能减少 |
| D、构成的原电池或电解池工作后都会产生大量气体 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.如果为原电池,铜易失电子而作负极,银作正极,正极上电解质溶液中阳离子得电子发生还原反应;
B.如果构成电解池,阳极上金属材料失电子而导致金属材料质量减少;
C.如果构成电解池,阳极上金属材料失电子而导致金属材料质量减少;
D.构成原电池或电解池,根据各个电极上放电物质分析解答.
B.如果构成电解池,阳极上金属材料失电子而导致金属材料质量减少;
C.如果构成电解池,阳极上金属材料失电子而导致金属材料质量减少;
D.构成原电池或电解池,根据各个电极上放电物质分析解答.
解答:
解:A.如果为原电池,铜易失电子而作负极,银作正极,正极上电极反应式为Ag++e-=Ag,故A错误;
B.如果构成电解池,阳极上金属材料失电子而导致金属材料质量减少,a电极可能是阳极也可能是阴极,如果是阳极则质量会减少,如果是阴极则质量增加,故B错误;
C.如果构成电解池,b电极可能是阳极也可能是阴极,如果是阳极则质量会减少,如果是阴极则质量增加,故C正确;
D.构成原电池时负极上铜失电子生成铜离子,正极上银离子放电生成银,构成电解池时,阳极上金属失电子,阴极上金属离子得电子,所以无论是原电池还是电解池都得不到气体,故D错误;
故选C.
B.如果构成电解池,阳极上金属材料失电子而导致金属材料质量减少,a电极可能是阳极也可能是阴极,如果是阳极则质量会减少,如果是阴极则质量增加,故B错误;
C.如果构成电解池,b电极可能是阳极也可能是阴极,如果是阳极则质量会减少,如果是阴极则质量增加,故C正确;
D.构成原电池时负极上铜失电子生成铜离子,正极上银离子放电生成银,构成电解池时,阳极上金属失电子,阴极上金属离子得电子,所以无论是原电池还是电解池都得不到气体,故D错误;
故选C.
点评:本题考查了原电池和电解池原理,明确离子放电顺序是解本题关键,注意活泼金属作电解池阳极时,阳极上金属材料失电子而不是电解质溶液中阴离子失电子,为易错点.

练习册系列答案
相关题目
下列离子方程式正确的是( )
| A、将铝片加入少量烧碱溶液中:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
| B、利用醋酸溶解含碳酸钙的水垢:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C、铁屑溶于过量稀硝酸:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O |
| D、FeI2溶液中通入少量氯气:2Fe2++Cl2=2Fe3++2Cl- |
101kpa,120℃,1L丁烷与氧气共V L点燃,产物无单质,产物通过碱石灰,体积减少8L,温度保持不变,剩余气体体积为n L,剩余气体为m,则n和m分别是( )
| A、1,CO |
| B、2,CO2 |
| C、2,H2 |
| D、1,H2O |
物质的量浓度都为0.1mol/L的下列溶液中,pH最小的是( )
| A、NH4Cl |
| B、NaCl |
| C、CH3COONa |
| D、NaNO3 |
等物质的量的下列物质完全燃烧时,消耗氧气的量最多的是( )
| A、C3H4 |
| B、C2H6 |
| C、C2H6O |
| D、C2H4O2 |