题目内容
A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20.其中A为非金属元素,C是金属元素;A、C元素原子的最外层都只有一个电子;B和D元素原子的最外层电子数相同,且B元素原子L层电子数是K层电子数的3倍;E元素原子最外层电子数比次外层电子数少1.回答下列问题:
(1)写出五种元素的元素符号:
A. ,B. ,C. ,D. ,E. .
(2)画出B、C的原子结构示意图:B. ,C. ;画出D的离子结构示意图: .
(3)从原子核外电子排布的角度分析C元素的化合价为+1价的原因 .
(1)写出五种元素的元素符号:
A.
(2)画出B、C的原子结构示意图:B.
(3)从原子核外电子排布的角度分析C元素的化合价为+1价的原因
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20,B和D元素原子的最外层电子数相同,二者处于同主族,且B原子L层电子数是K层电子数的3倍,则B原子L层电子数为6,则B为氧元素、D为硫元素;
C是金属元素,A和C原子的最外层电子都只有一个,二者处于ⅠA族,结合原子序数可知,A为氢元素、C为钠元素;E元素原子的最外层电子数比次外层电子数少1,即最外层为7,故E为氯元素,据此解答各小题即可.
C是金属元素,A和C原子的最外层电子都只有一个,二者处于ⅠA族,结合原子序数可知,A为氢元素、C为钠元素;E元素原子的最外层电子数比次外层电子数少1,即最外层为7,故E为氯元素,据此解答各小题即可.
解答:
解:依据分析可知:A为氢,B为氧,C为钠,D为硫,E为氯,
(1)依据分析可知:A为氢,B为氧,C为钠,D为硫,E为氯,元素符号依次为:H、O、Na、S、Cl,故答案为:H、O、Na、S、Cl;
(2)O原子有两个电子层,最外层6个电子结构示意图为: ,Na原子有3个电子层,最外层1个电子,故Na原子结构示意图为:
,Na原子有3个电子层,最外层1个电子,故Na原子结构示意图为: ,S得到2个电子形成最外层8个电子的稳定结构,故S离子结构示意图为:
,S得到2个电子形成最外层8个电子的稳定结构,故S离子结构示意图为: ,故答案为:
,故答案为: ;
; ;
; ;
;
(3)钠元素核外电子排布原子核外电子排布是第一层2个电子,第二层8个电子,最外层1个电子,故钠容易失去最外层的一个电子,形成最外层8个电子的稳定结构,+1价所以钠元素的化合价是+1价,故答案为:钠容易失去最外层的一个电子,形成最外层8个电子的稳定结构.
(1)依据分析可知:A为氢,B为氧,C为钠,D为硫,E为氯,元素符号依次为:H、O、Na、S、Cl,故答案为:H、O、Na、S、Cl;
(2)O原子有两个电子层,最外层6个电子结构示意图为:
 ,Na原子有3个电子层,最外层1个电子,故Na原子结构示意图为:
,Na原子有3个电子层,最外层1个电子,故Na原子结构示意图为: ,S得到2个电子形成最外层8个电子的稳定结构,故S离子结构示意图为:
,S得到2个电子形成最外层8个电子的稳定结构,故S离子结构示意图为: ,故答案为:
,故答案为: ;
; ;
; ;
;(3)钠元素核外电子排布原子核外电子排布是第一层2个电子,第二层8个电子,最外层1个电子,故钠容易失去最外层的一个电子,形成最外层8个电子的稳定结构,+1价所以钠元素的化合价是+1价,故答案为:钠容易失去最外层的一个电子,形成最外层8个电子的稳定结构.
点评:本题难度不大,考查学生对原子符号、原子(离子)结构示意图及其意义的理解,了解原子符号的意义是正确解题的关键.

练习册系列答案
相关题目
下列各组中两种物质在溶液中的反应,可用同一离子方程式表示的是( )
| A、Cu(OH)2+HCl;NaOH+HNO3 |
| B、NaHCO3+H2SO4;Na2CO3+HCl |
| C、NaHSO4+NaOH;H2SO4+NaOH |
| D、BaCl2+H2SO4;Ba(OH)2+H2SO4 |
最近江苏省大部分地区遭受严重的雾霾天气,雾霾属于哪种分散系( )
| A、溶液 | B、胶体 |
| C、乳浊液 | D、悬浊液 |
 已知某可逆反应在密闭容器中进行:A(g)+2B(g)?3C(g)△H>0,如图中曲线a代表一定条件下该反应的过程,若使a曲线变为b曲线,可采取的措施是( )
已知某可逆反应在密闭容器中进行:A(g)+2B(g)?3C(g)△H>0,如图中曲线a代表一定条件下该反应的过程,若使a曲线变为b曲线,可采取的措施是( )| A、恒温恒容条件下将A、B的浓度增加一倍 |
| B、恒温条件下加压(缩小容器体积) |
| C、使用合适的催化剂 |
| D、升高温度 |
短周期元素R、T、X、Y、Z在元素周期表的相对位置如下表所示,它们的最外层电子数之和为24.则下列判断正确的是( )
| R | T | |
| X | Y | Z |
| A、气态氢化物稳定性:Y>T |
| B、五种元素中原子半径最大的是Z |
| C、R位于元素周期表中第二周期第ⅣA族 |
| D、Z元素的最高价氧化物对应的水化物的化学式为HZO4 |
下列化合物的分子中,所有原子都处于同一平面的有( )
| A、乙烷 | B、甲苯 |
| C、丙炔 | D、四氯乙烯 |
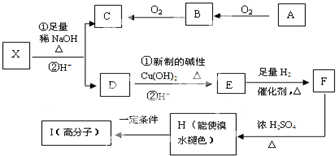
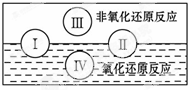 已知元素X、Y、Z质子数都小于18,并且质子数X+Y=Z.X原子的电子层数与核外电子总数相同,Z原子有两个电子层,最外层电子数是内层电子数的三倍,则:
已知元素X、Y、Z质子数都小于18,并且质子数X+Y=Z.X原子的电子层数与核外电子总数相同,Z原子有两个电子层,最外层电子数是内层电子数的三倍,则: