题目内容
9.在500℃、2×107Pa和催化剂条件下,把物质A,B按物质的量之比2:1充入固定容积为2L的密闭容器中,发生如下反应:2A(g)+B(g)?2C(g)△H=-180kJ•mol-1(1)写出该反应的化学平衡常数表达式K=$\frac{{c}^{2}(C)}{{c}^{2}(A)c(B)}$.
(2)降低温度,该反应K值增大,化学反应速率减小(以上均填“增大,减小或不变”)
(3)在此条件下向此容器中充入2molA和过量的B,充分反应后,放出的热量<180kJ (填“<”“>”“=”),理由该反应为可逆反应,有一定的限度,不能进行到底.
(4)关于该反应的下列说法中,正确的是D
A.△H>0,△S>0B.△H>0,△S<0
C.△H<0,△S>0D.△H<0,△S<0
(5)在上述反应条件的密闭容器中,欲提高A和B的转化率,下列措施可靠的是AD(多选)
A.向容器中按原比例再充入原料气 B.向容器中再充入惰性气体
C.改变反应的催化剂 D.分离出物质C.
分析 (1)平衡常数等于生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积;
(2)反应是放热反应降低温度平衡逆向进行,反应速率减小;
(3)反应是可逆反应不能进行彻底;
(4)反应焓变小于0,△H<0,反应前后气体体积减小熵变△S<0;
(5)反应条件的密闭容器中欲提高AB的转化率,应使平衡正向移动,据此回答.
解答 解:(1)平衡常数等于生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积,2A(g)+B(g)?2C(g),平衡常数K=$\frac{{c}^{2}(C)}{{c}^{2}(A)c(B)}$,
故答案为:$\frac{{c}^{2}(C)}{{c}^{2}(A)c(B)}$;
(2)反应是放热反应,降低温度平衡逆向进行,平衡常数减小,化学反应速率减小,
故答案为:增大,减小;
(3)2A(g)+B(g)?2C(g)△H=-180kJ•mol-1,焓变是2molA和1molB完全反应生成2molC放热180KJ,在此条件下向此容器中充入2molA和过量的B,反应是可逆反应,充分反应后,放出的热量小于180KJ,
故答案为:<,该反应为可逆反应,有一定的限度,不能进行到底;
(4)反应焓变小于0,△H<0,反应前后气体体积减小熵变△S<0,选D,
故答案为:D;
(5)根据化学平衡:2A(g)+B(g)?2C(g)△H=-180kJ•mol-1,反应是气体体积减小的放热反应,欲提高AB的转化率,平衡正向进行;
A.向容器中按原比例再充入原料气,则压强增大,平衡向右移动,AB的转化率增大,故A正确;
B.向容器中再充入惰性气体,总压增大分压不变,则各组分浓度不变,平衡不移动,AB的转化率不变,故B错误;
C.改变反应的催化剂,不影响平衡的移动,AB的转化率不变,故C错误;
D.液化生成物分离出氨,平衡向右移动,AB的转化率增大,故D正确;
故答案为:AD.
点评 本题考查平衡常数表达、化学反应速率、影响化学平衡的因素与平衡状态的判断等,属于综合的考查,注意知识的归纳和整理是解题关键,题目难度中等.

 名题金卷系列答案
名题金卷系列答案| 选项 | 化学式 | 电子式或含有的化学键类型 | 物质的性质 | 与性质相对应的用途 |
| A | NaClO | 离子键 共价键 | 强氧化性 | 消毒剂 |
| B | H2O2 | 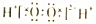 | 不稳定,易分解 | 医用消毒剂 |
| C | NH3 | 共价键 | 水溶液呈弱碱性 | 工业制硝酸 |
| D | NaHCO3 | 离子键 | 受热易分解 | 泡沫灭火器 |
| A. | A | B. | B | C. | C | D. | D |
| 选项 | 实验操作 | 实验目的 |
| A | 向甲酸钠溶液中加新制的Cu(OH)2并加热 | 确定甲酸钠具有醛基性质 |
| B | 加溴水,振荡,过滤除去沉淀 | 除去苯中混有的苯酚 |
| C | 给碳酸钠溶液中加入浓盐酸,将产生的气体通入苯酚钠溶液 | 验证酸性: 盐酸>碳酸>苯酚 |
| D | 氯乙烷和氢氧化钠的乙醇溶液共热,将产生的气体通入酸性高锰酸钾溶液 | 验证产生的气体为乙烯 |
| A. | A | B. | B | C. | C | D. | D |
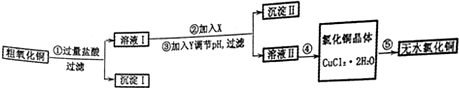
已知:
| 金属离子 | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
(1)步骤②反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.步骤③中调节溶液pH的范围是3.2~4.7之间.
(2)如何判断沉淀Ⅱ已洗涤干净的方法是取最后一次洗涤液,加入硝酸酸化,再滴入硝酸银溶液,没有白色沉淀生成,说明洗涤干净,否则洗涤不干净.
(3)步骤④的方法是加热浓缩、冷却结晶、过滤、洗涤,
(4)步骤⑤要得到无水氯化铜,需要在赶在的HCl气流中加热CuCl2•2H2O其原因是干燥的HCl气流既可抑制Cu2+的水解,还能带走CuCl2•2H2O受热产生的水汽.
(5)若用电解法精炼铜,则阴极的电极反应式为Cu2++2e-=Cu.
| A. | 饱和食盐水中:c(Na+)+c(H+)=c(Cl-)+c(OH-) | |
| B. | 饱和小苏打溶液中:c(Na+)=c(HCO3-) | |
| C. | pH=4的醋酸中:c(H+)=4.0mol•L-1 | |
| D. | pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol•L-1 |
| A. | 2C2H2(g)+5O2(g)→4CO2(g)+2H2O(l)+129.96kJ | |
| B. | 2C2H2(g)+5O2(g)→4CO2(g)+2H2O(g)-259.92kJ | |
| C. | 2C2H2(g)+5O2(g)→4CO2(g)+2H2O(l)-1299.6kJ | |
| D. | 2C2H2(g)+5O2(g)→4CO2(g)+2H2O(l)+2599.2kJ |
 ;写出A分子中官能团的名称羟基、羧基;
;写出A分子中官能团的名称羟基、羧基; ;
;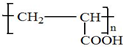 .
.
 .
.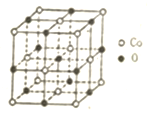 汽车安全气囊一般由传感器、气囊、气体发生器等组成.
汽车安全气囊一般由传感器、气囊、气体发生器等组成.