题目内容
NA表示阿伏加德罗常数,列各项正确的是( )
| A、1 mol?L-1 NaCl溶液含有NA个Na+ |
| B、标准状况下,分子数为NA的CO、N2的混合气体体积约为22.4 L,质量为28 g |
| C、标准状况下,22.4 L空气含有NA个单质分子 |
| D、22.4 L O2所含的原子数为2NA |
考点:阿伏加德罗常数
专题:
分析:A、溶液体积不明确;
B、根据V=nVm和m=nM来计算;
C、空气是多种化合物和单质的混合物;
D、状态不明确.
B、根据V=nVm和m=nM来计算;
C、空气是多种化合物和单质的混合物;
D、状态不明确.
解答:
解:A、溶液体积不明确,故无法计算溶液中Na+的个数,故A错误;
B、混合气体的物质的量n=
=
=1mol,气体的体积V=nVm=1mol×22.4L/mol=22.4L;CO、N2的摩尔质量均为28g/mol,故混合气体的质量m=nM=1mol×28g/mol=28g,故B正确;
C、标准状况下,22.4 L空气的物质的量为1mol,而空气是多种化合物和单质的混合物,不单是单质分子,故单质分子的个数小于NA个,故C错误;
D、状态不明确,故22.4 L O2不一定是1mol,故D错误.
故选B.
B、混合气体的物质的量n=
| N |
| NA |
| NA |
| NA |
C、标准状况下,22.4 L空气的物质的量为1mol,而空气是多种化合物和单质的混合物,不单是单质分子,故单质分子的个数小于NA个,故C错误;
D、状态不明确,故22.4 L O2不一定是1mol,故D错误.
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A、标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为7/22.4NA |
| B、1 mol甲基(-CH3)所含的电子总数为9NA |
| C、0.5 摩1,3-丁二烯分子中含有C=C双键数为 NA |
| D、1 mol碳正离子(CH+3)所含的电子总数为8NA |
NA为阿伏加德罗常数的数值,下列对0.3mol?L-的Na2SO4 溶液的说法中,正确的是( )
| A、0.3molNa2SO4溶于1 L水即得该溶液 |
| B、1L该溶液中含有0.6 NA个Na+和0.3NA个SO42- |
| C、1L该溶液中Na+的物质的量浓度为0.3mol?L-1 |
| D、取10L该溶液,其物质的量浓度为3mol?L-1 |
生产重铬酸钠(Na2Cr2O7?2H2O)的主要反应为( )
(1)4(FeO?Cr2O3)+8Na2CO3+7O28Na2
CrO4+2Fe2O3+8CO2
(2)2Na2CrO4+H2SO4?Na2SO4+Na2Cr2O7+H2O,下列说法正确的是.
(1)4(FeO?Cr2O3)+8Na2CO3+7O28Na2
| ||
(2)2Na2CrO4+H2SO4?Na2SO4+Na2Cr2O7+H2O,下列说法正确的是.
| A、反应(1)和(2)均为氧化还原反应 |
| B、(1)中被还原的元素为O,被氧化的元素只有Fe |
| C、反应(2)中氧化产物与还原产物的物质的量之比为1:1 |
| D、反应(1)中每生成1molNa2CrO4时电子转移3.5mol |
铁和水蒸气在高温条件下发生反应3Fe+4H2O(g)
Fe3O4+4H2,在此反应中水是( )
| ||
| A、氧化剂 |
| B、还原剂 |
| C、既是氧化剂又是还原剂 |
| D、既不是氧化剂又不是还原剂 |
下列物理量中,不能由阿伏加德罗常数(NA)、一个水分子的质量(m水)和一个水分子的体积(V水)确定的是( )
| A、1 mol液态水的质量 |
| B、1 mol水蒸气的质量 |
| C、1 mol液态水的体积 |
| D、1 mol水蒸气的体积 |
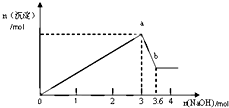 有一无色透明溶液,可能含Al3+、Fe3+、Mg2+、Na+、CO32-、Cl-、NO3-等离子中的若干种.现做如下实验:
有一无色透明溶液,可能含Al3+、Fe3+、Mg2+、Na+、CO32-、Cl-、NO3-等离子中的若干种.现做如下实验: