题目内容
现有如下两个反应:(A)NaOH+HCl═NaCl+H2O (B)2FeCl3+Cu═2FeCl2+CuCl2
(1)根据能设计成原电池的反应选择适宜的材料和试剂设计一个原电池:请画原电池装置示意图(注明电极正负极、电极材料、电解质溶液)
(2)常用来冶炼该电池负极材料的两种方法是(用化学方程式表示) 、 .
(1)根据能设计成原电池的反应选择适宜的材料和试剂设计一个原电池:请画原电池装置示意图(注明电极正负极、电极材料、电解质溶液)
(2)常用来冶炼该电池负极材料的两种方法是(用化学方程式表示)
考点:设计原电池,金属冶炼的一般原理
专题:电化学专题,金属概论与碱元素
分析:(1)能设计成原电池的反应必须是能自发进行的放热的氧化还原反应,根据方程式知,B能设计成原电池,Cu失电子化合价升高而作负极,则不如Cu活泼的金属或导电的非金属作正极,氯化铁溶液为电解质溶液;
(2)Cu属于较活泼金属,采用火法或湿法冶炼铜.
(2)Cu属于较活泼金属,采用火法或湿法冶炼铜.
解答:
解:(1)能设计成原电池的反应必须是能自发进行的放热的氧化还原反应,根据方程式知,B能设计成原电池,Cu失电子化合价升高而作负极,则不如Cu活泼的金属或导电的非金属作正极,氯化铁溶液为电解质溶液,该装置图为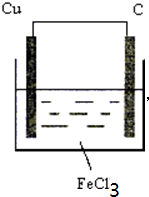 ,故答案为:
,故答案为: ;
;
(2)Cu属于较活泼金属,采用火法或湿法冶炼铜,采用火法冶炼方程式为Cu2S+O2
2Cu+SO2,采用湿法冶炼方程式为Fe+CuSO4=FeSO4+Cu,故答案为:Cu2S+O2
2Cu+SO2(火法炼铜);Fe+CuSO4=FeSO4+Cu(湿法炼铜).
 ,故答案为:
,故答案为: ;
;(2)Cu属于较活泼金属,采用火法或湿法冶炼铜,采用火法冶炼方程式为Cu2S+O2
| ||
| ||
点评:本题考查了原电池设计,根据方程式知元素化合价变化确定负极、电解质溶液,再结合金属的活泼性、物质的导电性确定正极,根据金属的活泼性强弱确定金属的冶炼方法,题目难度不大.

练习册系列答案
相关题目
0.1mol?L-1某酸HA溶液的pH=2,则该溶液中有关浓度关系式正确的是( )
| A、c(H+)>c(A-) |
| B、c(H+)>c(HA) |
| C、c(OH-)>c(HA) |
| D、c(HA)>c(A-) |
下列化合物的电子式书写错误的是( )
A、氨气  |
B、四氯化碳  |
C、次氯酸 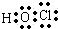 |
D、氯化钙  |
 如图,A是一种非金属单质,E是一种白色沉淀.据图填空:
如图,A是一种非金属单质,E是一种白色沉淀.据图填空: (1)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.图是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式
(1)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.图是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式