题目内容
19.能正确表示下列反应的离子方程式为( )| A. | 硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ | |
| B. | 少量的NaOH溶液滴入NH4HCO3溶液中:HCO3-+OH-=CO32-+H2O | |
| C. | 少量SO2通入苯酚钠溶液中:C6H5O-+SO2+H2O=C6H5OH+HSO3- | |
| D. | 大理石溶于醋酸中:CaCO3+2H+=Ca2++CO2↑+H2O |
分析 A.发生氧化还原反应生成硝酸铁、NO、S和水;
B.少量NaOH,只与碳酸氢根离子反应;
C.反应生成苯酚和亚硫酸钠;
D.醋酸在离子反应中保留化学式.
解答 解:A.硫化亚铁具有还原性,而硝酸具有氧化性,两者要发生氧化还原反应,离子反应为FeS+4H++NO3-=Fe3++S↓+NO↑+2H2O,故A错误;
B.少量的NaOH溶液滴入NH4HCO3溶液中的离子反应为HCO3-+OH-=CO32-+H2O,故B正确;
C.少量SO2通入苯酚钠溶液中的离子反应为2C6H5O-+SO2+H2O=2C6H5OH+SO32-,故C错误;
D.大理石溶于醋酸中的离子反应为CaCO3+2CH3COOH=Ca2++CO2↑+H2O+2CH3COO-,故D错误;
故选B.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.下列说法正确的是( )
| A. | P4和NO2都是共价化合物 | |
| B. | 在CO2和SiO2晶体中都存在分子间作用力 | |
| C. | CCl4和NH3分子中都含有极性键 | |
| D. | Na2O2是离子化合物,只含有离子键 |
10.一种比黄金还要贵重百倍的${\;}_{8}^{18}$O2气体,不久前在我国兰州近代物理研究所制备成功,1mol这种${\;}_{8}^{18}$O2气体所含有的中子的物质的量为( )
| A. | 36mol | B. | 20mol | C. | 16mol | D. | 20NA |
7.下列操作不能达到目的是( )
| 选项 | 目的 | 操作 |
| A | 确定NaCl溶液中是否混有Na2CO3 | 取少量溶液滴加CaCl2溶液,观察是否出现白色浑浊 |
| B | 除去KNO3中少量NaCl | 将混合物制成热的饱和溶液,冷却结晶,过滤 |
| C | 除去硫酸钡固体中的碳酸钡 | 向盛有足量盐酸的烧杯中加入该固体,用玻璃棒不断搅拌并充分浸泡,静置,过滤,洗涤,烘干 |
| D | 配制100mL1.0mol/LCuSO4溶液 | 将25gCuSO4•5H2O溶于100mL蒸馏水中 |
| A. | A | B. | B | C. | C | D. | D |
4.近年来科学家发现维生素C(C6H8O6)有防癌作用,下列关于维生素C的说法中不正确的是( )
| A. | 维生素C是有机物 | |
| B. | 一个维生素C分子中含有20个原子 | |
| C. | 一个维生素C分子由碳、氢、氧三种元素组成 | |
| D. | 某些蔬菜、水果中富含维生素C |
10.蛇纹石矿可以看做是由MgO、Fe2O3、Al2O3、SiO2组成.由蛇纹石制取碱式碳酸镁的实验步骤如下:
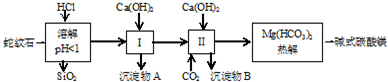
(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是Fe3+、Al3+.
(2)进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见表)
Ca(OH)2不能过量,若Ca(OH)2过量可能会导致Al(OH)3溶解、Mg(OH)2沉淀生成.
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入过量NaOH(填入物质的化学式),然后过滤、洗涤、灼烧 (依次填写实验操作名称).
(4)Mg(HCO3)2热分解的反应方程式为:2 Mg(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$Mg2(OH)2CO3+3CO2↑+H2O.若热分解不完全,所得碱式碳酸镁中将混有MgCO3,则产品中镁的质量分数降低(填“升高”、“降低”或“不变”,已知碳酸镁的相对分子质量为84,碱式碳酸镁的相对分子质量为142).
(5)上述实验中,可以循环使用的物质是CO2(填写物质化学式).
(6)除去MgCl2酸性溶液中的Fe3+,可在加热、搅拌的条件下加入MgO或Mg(OH)2或MgCO3(试剂自选),过滤后再加入适量盐酸.

| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
(2)进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见表)
Ca(OH)2不能过量,若Ca(OH)2过量可能会导致Al(OH)3溶解、Mg(OH)2沉淀生成.
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入过量NaOH(填入物质的化学式),然后过滤、洗涤、灼烧 (依次填写实验操作名称).
(4)Mg(HCO3)2热分解的反应方程式为:2 Mg(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$Mg2(OH)2CO3+3CO2↑+H2O.若热分解不完全,所得碱式碳酸镁中将混有MgCO3,则产品中镁的质量分数降低(填“升高”、“降低”或“不变”,已知碳酸镁的相对分子质量为84,碱式碳酸镁的相对分子质量为142).
(5)上述实验中,可以循环使用的物质是CO2(填写物质化学式).
(6)除去MgCl2酸性溶液中的Fe3+,可在加热、搅拌的条件下加入MgO或Mg(OH)2或MgCO3(试剂自选),过滤后再加入适量盐酸.