题目内容
16.将1LpH=13 的氨水溶液加入水稀释到10.0L后,下列微粒浓度增大的是( )| A. | c[NH3•H2O] | B. | c[H+] | C. | c[OH-] | D. | c[NH4+] |
分析 加水稀释氨水,会促进一水合氨的电离,但是由于溶液的体积增大的程度大于氢离子的物质的量增大程度,所以溶液中氢离子浓度减小,结合Kw分析.
解答 解:A.加水稀释氨水,会促进一水合氨的电离,则c[NH3•H2O]减小,故A不选;
B.加水稀释氨水,会促进一水合氨的电离,但是由于溶液的体积增大的程度大于氢离子的物质的量增大程度,所以溶液中氢离子浓度减小,故B不选;
C.由于温度不变,所以Kw=c[H+]×c[OH-]的值不变,氢离子浓度减小,所以c[OH-]增大,故C选;
D.加水稀释氨水,会促进一水合氨的电离,但是由于溶液的体积增大的程度大于铵根离子的物质的量增大程度,所以c[NH4+]减小,故dD不选.
故选C.
点评 本题考查了弱电解质的电离平衡,题目难度不大,注意把握弱电解质的电离平衡的特点和影响因素,侧重于考查学生的分析能力.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案
相关题目
7.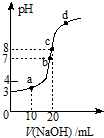 常温时,用0.10mol/L的NaOH溶液滴定20.00mL 0.10mol/L某 一元酸HA溶液所得滴定曲线如图.下列说法不正确的是( )
常温时,用0.10mol/L的NaOH溶液滴定20.00mL 0.10mol/L某 一元酸HA溶液所得滴定曲线如图.下列说法不正确的是( )
 常温时,用0.10mol/L的NaOH溶液滴定20.00mL 0.10mol/L某 一元酸HA溶液所得滴定曲线如图.下列说法不正确的是( )
常温时,用0.10mol/L的NaOH溶液滴定20.00mL 0.10mol/L某 一元酸HA溶液所得滴定曲线如图.下列说法不正确的是( )| A. | a、b、c三点所示溶液导电能力最强的是c点对应的溶液 | |
| B. | 在c点溶液中:c(H+)+c(HA)=c(OH-) | |
| C. | 25℃,HA的电离平衡常数约为1.0×10-5 | |
| D. | a、b、c、d四点所示溶液中水的电离程度最大的是b点对应的溶液 |
4.在下列各组物质中,属于同系物的一组是( )
| A. | 1,1-二溴乙烷和1,2-二溴乙烷 | B. | 苯和甲苯 | ||
| C. | 乙二醇和丙三醇 | D. | 乙烯和环丙烷 |
11.下列指定溶液中一定能大量共存的离子组是( )
| A. | pH=1的溶液中:NH4+、Na+、Fe3+、SO42- | |
| B. | 中性溶液中:K+、Fe3+、Cl-、SO42- | |
| C. | AlO2一的浓度为0.1 mol/L的溶液中:K+、Na+、HCO3-、SO42- | |
| D. | Na2S溶液中:SO42-、K+、Cu2+、Cl- |
1.25℃时,用浓度为0.1000mol/L的氢氧化钠溶液分别滴定20.00mL浓度均为0.l000mol/L的二种酸HX、HY(忽略体积变化),实验数据如下表,下列判断不正确的是( )
| 数据编号 | 滴入NaOH(aq)的体积/mL | 溶液的pH | |
| HX | HY | ||
| ① | 0 | 3 | 1 |
| ② | a | 7 | x |
| ③ | 20.00 | >7 | y |
| A. | 在相同温度下,同浓度的两种酸溶液的导电能力:HX<HY | |
| B. | 由表中数据可估算出Ka(HX)≈10-5 | |
| C. | HY和HX混合,c(H+)=c(X-)+c(Y-)+c(OH-) | |
| D. | 上述②反应后的HY溶液中:c(Na+)>c(Y-)>c(OH-)>c(H+) |
8.下列物质与水反应生成强酸的是( )
| A. | Na2O | B. | SO3 | C. | CO2 | D. | NO |
5.下列实验合理的是( )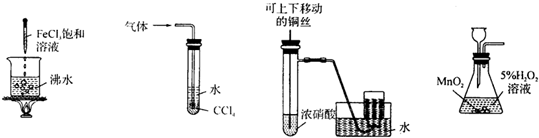

| A. | 得到红褐色沉淀 | B. | 吸收氨气,并防止倒吸 | ||
| C. | 制备并收集少量NO2气体 | D. | 实验室制O2 |
6.14C常用于测定生物遗骸的年份.下列说法中正确的是( )
| A. | 14C的质量数为14g•mol-1 | B. | 14C与12C是两种不同的元素 | ||
| C. | 14C与C60互为同素异形体 | D. | 14C与14N中子数一定不同 |