题目内容
15.如表列出了周期表短周期中6种元素的有关数据:| 元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 原子半径(nm) | 0.075 | 0.110 | 0.152 | 0.071 | 0.186 | 0.099 |
| 最高价态 | +5 | +5 | +1 | 0 | +1 | +7 |
| 最低价态 | -3 | -3 | 0 | -1 | 0 | -1 |
(1)写出上述编号对应元素的元素符号:②P
(2)元素④在周期表中的位置是第二周期第 VIIA族.
(3)元素⑤形成的两种常见氧化物的化学式分别为Na2O、Na2O2,其中都含有的化学键是离子键.
(4)①的氢化物和⑥的氢化物反应的化学方程式为NH3+HCl=NH4Cl.
分析 由表格中数据可知,①②位于ⅤA族,①的原子半径小,则①为N,②为P;④⑥的最外层电子数均为7,且F无正价,则④为F,⑥为Cl;③⑤均只有+1价,均为IA族元素,结合原子半径可知,③为Li,⑤为Na,以此来解答.
解答 解:由上述分析可知,①为N,②为P,③为Li,④为F,⑤为Na,⑥为Cl,
(1)②为P,故答案为:P;
(2)元素④在周期表中的位置是第二周期第 VIIA族,故答案为:第二周期第 VIIA族;
(3)元素⑤形成的两种常见氧化物的化学式分别为Na2O、Na2O2,均含离子键,故答案为:Na2O;Na2O2;离子键;
(4)①的氢化物和⑥的氢化物反应的化学方程式为NH3+HCl=NH4Cl,故答案为:NH3+HCl=NH4Cl.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子半径、元素的化合价来推断元素为解答关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
5.下列叙述正确的是( )
| A. | 金刚石和石墨互称同位素 | B. | 甲烷和异丁烷互称同系物 | ||
| C. | 医用消毒酒精中乙醇的浓度为95% | D. | 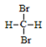 和 和  互称同分异构体 互称同分异构体 |
6.下列有关化学用语使用正确的是( )
| A. | 硫原子的原子结构示意图: | |
| B. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O | |
| C. | NH4Cl的电子式: | |
| D. | 用电子式表示氯化氢分子的形成过程: |
3.下述实验能达到预期目的是( )
| 编号 | 实验内容 | 实验目的 |
| A | 将Na2CO3和NaHCO3的固体混合物加热灼烧 | 除去NaHCO3中的Na2CO3 |
| B | 常温时将CO通过装有SiO2的硬质玻璃管 | 制取粗硅 |
| C | 向新制得的K2S溶液中滴加新制的氯水 | 比较氯与硫的得电子能力 |
| D | 分别向2支盛有冷水的试管中加入相同大小的镁条和铝条 | 比较镁铝的金属性强弱 |
| A. | A | B. | B | C. | C | D. | D |
20.下列实验操作,实验现象与结论对应关系正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,然后加入适量稀NaOH溶液,再向其中加入新制的银氨溶液,并水浴加热 | 有银镜生成 | 蔗糖已经完全水解为具有还原性的葡萄糖 |
| B | 检验HCl气体中是否含有CO2,可将气体通入Ca(OH)2溶液中 | 没有出现白色沉淀 | 证明不含有CO2 |
| C | 强酸性溶液X中加入Ba(NO3)2溶液,静置后再加入KSCN溶液 | 先有白色沉淀,后溶液又变红 | X中一定含有SO42-和Fe3+ |
| D | 检验HCl气体中是否含有Cl2,可将气体通入品红溶液中,然后加热 | 品红溶液褪色,加热后溶液不恢复成红色 | 证明含有Cl2 |
| A. | A | B. | B | C. | C | D. | D |
7.下列实验所用试剂、现象和结论均正确的是( )
| 序号 | 相关实验 | 试剂 | 现象和结论 |
| ① | 鉴别K2CO3和Na2SO4 | 稀硫酸、澄清石灰水 | 产生使澄清石灰水变浑浊的无色无味气体的是K2CO3 |
| ② | 鉴别NO2和Br2蒸汽 | 湿润的淀粉KI试纸 | 试纸变蓝色的是Br2蒸汽 |
| ③ | 鉴别葡萄糖和蔗糖 | 银氨溶液 | 有银镜产生的是葡萄糖 |
| ④ | 鉴别AlCl3溶液和MgCl2溶液 | 氨水 | 先产生白色沉淀,然后沉淀又消失的是AlCl3溶液 |
| A. | ①③ | B. | ①② | C. | ②④ | D. | ②③ |
4.恒温下向体积为5L的恒容密闭容器中通入2mol A气体和1mol B气体,发生如下反应:2A(g)+B(g)?x C(g),2min时反应达到平衡状态,此时A的转化率和C的体积分数都是25%.则能作为该可逆反应到达平衡的标志是( )
| A. | 混合气体平均相对分子质量保持一定 | |
| B. | 单位时间内每生成3mol C的同时,生成1 mol B | |
| C. | 容器内气体密度恒定不变 | |
| D. | 反应前后容器内总压强恒定不变 |