题目内容
下列离子方程式正确的是( )
| A、把Fe(OH)3放入氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O | ||||
B、Mg (HCO3)2溶液和足量的澄清石灰水反应:Mg2++2HCO
| ||||
C、Ca(HCO3)2溶液和过量NaOH溶液反应:Ca2++2HCO
| ||||
| D、把Mg粉放入FeCl3溶液中:2Fe3++3Mg+6H2O=2Fe(OH)3↓+3Mg2++3H2↑ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.二者反应生成亚铁离子和碘;
B.氢氧化镁的溶解性小于碳酸镁,所以生成氢氧化镁;
C.二者反应生成碳酸钙、碳酸钠和水;
D.发生氧化还原反应生成氯化镁和氯化亚铁.
B.氢氧化镁的溶解性小于碳酸镁,所以生成氢氧化镁;
C.二者反应生成碳酸钙、碳酸钠和水;
D.发生氧化还原反应生成氯化镁和氯化亚铁.
解答:
解:A.二者反应生成亚铁离子和碘,离子方程式为2Fe(OH)3+6H++2I-=I2+2Fe2++6H2O,故A错误;
B.氢氧化镁的溶解性小于碳酸镁,所以生成氢氧化镁,离子方程式为Mg2++2HCO3-+2Ca2++4OH-=2CaCO3↓+Mg(OH)2↓+2H2O,故B错误;
C.二者反应生成碳酸钙、碳酸钠和水,离子方程式为Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-,故C正确;
D.把镁粉放入FeCl3溶液中的离子反应为2Fe3++Mg═Mg2++2Fe2+,故D错误;
故选C.
B.氢氧化镁的溶解性小于碳酸镁,所以生成氢氧化镁,离子方程式为Mg2++2HCO3-+2Ca2++4OH-=2CaCO3↓+Mg(OH)2↓+2H2O,故B错误;
C.二者反应生成碳酸钙、碳酸钠和水,离子方程式为Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-,故C正确;
D.把镁粉放入FeCl3溶液中的离子反应为2Fe3++Mg═Mg2++2Fe2+,故D错误;
故选C.
点评:本题考查了离子方程式正误判断,为常考查题,注意把握反应实质,易错点为BD,题目难度中等.

练习册系列答案
相关题目
 用石墨电极电解CuCl2溶液(如图).下列分析不正确的是( )
用石墨电极电解CuCl2溶液(如图).下列分析不正确的是( )| A、a端是直流电源的负极 |
| B、通电使CuCl2发生电离 |
| C、阴极上发生的反应:Cu2++2e-=Cu |
| D、通电一段时间后,在阳极附近观察到黄绿色气体 |
有A、B、C三块金属片,进行如下实验,①A、B用导线相连后,同时插入稀H2SO4中,A极为负极;②A、C相连后,同时浸入稀H2SO4,C极发生氧化反应.则三种金属的活动性顺序为( )
| A、A>C>B |
| B、B>C>A |
| C、C>A>B |
| D、A>B>C |
NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、在常温常压下,14gN2和CO的混合气体所含原子数为NA |
| B、500mL 1 mol/L Na2SO3溶液中的钠离子数为0.5NA |
| C、盛有SO2的密闭容器中含有NA个氧原子,则SO2的体积为11.2L |
| D、22.4L氨气所含电子数为10NA |
在铁制品上镀上一定厚度的锌层,以下电镀方案中正确的是( )
| A、锌作阳极,铁制品作阴极,溶液中含Fe2+ |
| B、锌作阴极,铁制品作阳极,溶液中含Zn2+ |
| C、锌作阴极,铁制品作阳极,溶液中含Fe3+ |
| D、锌作阳极,铁制品作阴极,溶液中含Zn2+ |
在同温、同压下,11.5gA气体和8gO2分别刚好盛满同一不规则刚体容器,则气体A的相对分子质量为( )
| A、46g/mol | B、28g |
| C、44g/mol | D、46 |
下列说法正确的是( )
| A、向FeCl3溶液中加几滴KSCN,出现血红色沉淀 |
| B、Al的化学性质很活泼,所以Al不能直接放置空气中 |
| C、1molNaCl固体溶于1L水所得溶液中NaCl的物质的量浓度为1mol?L-1 |
| D、Al(OH)3可以来中和过多的胃酸 |
某氧化还原反应:A(g)+B(g)?2C(g)+D(s)△H<0,反应达到平衡后,在其他条件不变的情况下,下列说法正确的是( )
| A、加入催化剂,改变了反应的途径,反应的△H也随之改变 |
| B、改变压强,平衡不发生移动,反应放出的热量不变 |
| C、升高温度,反应速率加快,反应放出的热量不变 |
| D、若该反应在原电池中发生,达到平衡后测得放出的热量在数值上与△H相同 |
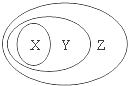 用如图表示的一些物质或概念间的从属关系中不正确的是( )
用如图表示的一些物质或概念间的从属关系中不正确的是( )