题目内容
下列叙述正确的是( )
| A、钢管与电源正极连接,可对钢管进行电化学保护 |
| B、利用高压氧舱治疗煤气中毒是依据平衡移动原理 |
| C、配制氯化亚锡(SnCl2)溶液时需加适量盐酸防止被氧化变浑浊 |
| D、用Fe除去溶液中的Cu2+、Hg2+与用FeS除去溶液中的Cu2+、Hg2+的原理相同 |
考点:金属的电化学腐蚀与防护,化学平衡的调控作用,难溶电解质的溶解平衡及沉淀转化的本质,溶液的配制
专题:
分析:A.作电解池阳极的金属加速被腐蚀,作电解池阴极的金属被保护;
B.煤气中毒病人血液中存在化学平衡CO(g)+Hb(O2)?O2(g)+Hb(CO);
C.SnCl2水解显酸性;
D.Fe与Cu2+、Hg2+发生置换反应,FeS与Cu2+、Hg2+发生沉淀的转化.
B.煤气中毒病人血液中存在化学平衡CO(g)+Hb(O2)?O2(g)+Hb(CO);
C.SnCl2水解显酸性;
D.Fe与Cu2+、Hg2+发生置换反应,FeS与Cu2+、Hg2+发生沉淀的转化.
解答:
解:A.作电解池阳极的金属加速被腐蚀,作电解池阴极的金属被保护,钢管与电源正极连接,钢管作电解池阳极,加速被腐蚀,故A错误;
B.煤气中毒病人血液中的化学平衡CO(g)+Hb(O2)?O2(g)+Hb(CO),CO中毒的病人置于高压氧舱,会使平衡逆向移动,让一氧化碳失去和血红蛋白结合的机会,故B正确;
C.SnCl2水解显酸性,配制氯化亚锡(SnCl2)溶液时需加适量盐酸防止发生水解变浑浊,故C错误;
D.Fe与Cu2+、Hg2+发生置换反应,属于氧化还原反应,FeS与Cu2+、Hg2+发生沉淀的转化,属于非氧化还原反应,原理不同,故D错误;
故选B.
B.煤气中毒病人血液中的化学平衡CO(g)+Hb(O2)?O2(g)+Hb(CO),CO中毒的病人置于高压氧舱,会使平衡逆向移动,让一氧化碳失去和血红蛋白结合的机会,故B正确;
C.SnCl2水解显酸性,配制氯化亚锡(SnCl2)溶液时需加适量盐酸防止发生水解变浑浊,故C错误;
D.Fe与Cu2+、Hg2+发生置换反应,属于氧化还原反应,FeS与Cu2+、Hg2+发生沉淀的转化,属于非氧化还原反应,原理不同,故D错误;
故选B.
点评:本题考查了金属的腐蚀与防护、平衡移动原理、盐的水解、沉淀的转化等,题目涉及的知识点较多,侧重于基础知识的综合应用的考查,题目难度中等.

练习册系列答案
相关题目
常温下,将pH=3的盐酸和pH=11的氨水等体积混合后,溶液中离子浓度关系是 ,而常温下,1mol?L-1的CH3COOH溶液与1mol?L-1的NaOH溶液等体积混合后,所得溶液中离子浓度关系是 .
在配制500ml 0.1mol/L的H2SO4溶液时,下列操作中会导致结果偏高的是( )
| A、洗净的容量瓶未经干燥就用于配制溶液 |
| B、未等溶液降至室温就转移至容量瓶 |
| C、转移溶液时不慎洒到容量瓶外 |
| D、定容时仰视刻度线 |
常温下,下列各组离子在指定的溶液中能大量共存的是( )
| A、滴入酚酞显红色的溶液:Na+、Al3+、SO42-、Cl- | ||
| B、滴入KSCN显红色的溶液:Na+、Cu2+、Br-、SO42- | ||
C、
| ||
D、c(H+)=
|
下列说法正确的是( )
| A、某芳香烃分子式为C9H12,其苯环上的一氯代物有两种的同分异构体有3种 |
| B、用溴水即可鉴别苯酚溶液、2,4-己二烯和甲苯 |
C、 分子中所有原子共平面 分子中所有原子共平面 |
D、1.0 mol 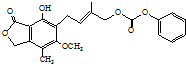 最多能与4.0 mol NaOH水溶液完全反应 最多能与4.0 mol NaOH水溶液完全反应 |