题目内容
7.下列关于原电池的叙述中,正确的是( )| A. | 原电池负极发生的电极反应是还原反应 | |
| B. | 原电池是将化学能转化为电能的装置 | |
| C. | 原电池在工作时其正极不断产生电子经外电路流向负极 | |
| D. | 原电池的电极只能由两种不同的金属构成 |
分析 原电池是把化学能转变为电能的装置,原电池放电时,负极上失去电子发生氧化反应,正极上得电子发生还原反应,电子从负极沿导线流下正极,电极材料可由金属构成,也可由能导电的非金属和金属材料构成.
解答 解:A、原电池负极上失电子发生氧化反应,故A错误;
B、原电池是把化学能转变为电能的装置,故B正确;
C、原电池在在工作时其负极不断产生电子并经外电路流向正极,故C错误;
D、原电池的电极可由两种不同的金属构成,也可由金属和能导电的非金属构成,故D错误.
故选B.
点评 本题考查了原电池原理,难度不大,会判断电子在外电路的流向及溶液中阴阳离子的移动方向.

练习册系列答案
相关题目
18.14C可用于考古,“14”是指( )
| A. | 质量数 | B. | 核外电子数 | C. | 中子数 | D. | 质子数 |
15.下列叙述中,错误的是( )
| A. | 苯与浓硝酸、浓硫酸共热并保持55℃-60℃反应生成硝基苯 | |
| B. | 苯在合适条件下催化加氢可生成环己烷 | |
| C. | 丙烯与溴的四氯化碳溶液反应生成1,2-二溴丙烷 | |
| D. | 甲苯与溴蒸气在光照条件下反应主要生成邻溴甲苯和对溴甲苯 |
2.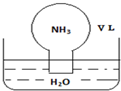 标准状况下,将体积为V L的圆底烧瓶中充满氨气,倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出,所得溶液的密度为ρg•cm-3.下列说法正确的是( )
标准状况下,将体积为V L的圆底烧瓶中充满氨气,倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出,所得溶液的密度为ρg•cm-3.下列说法正确的是( )
 标准状况下,将体积为V L的圆底烧瓶中充满氨气,倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出,所得溶液的密度为ρg•cm-3.下列说法正确的是( )
标准状况下,将体积为V L的圆底烧瓶中充满氨气,倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出,所得溶液的密度为ρg•cm-3.下列说法正确的是( )| A. | 条件不足,不能计算所得溶液的物质的量浓度 | |
| B. | 所得溶液中,n(NH3•H2O)+n(NH4+)=$\frac{V}{22.4}$ mol | |
| C. | 所得溶液的质量分数为$\frac{17}{22400}$ρ | |
| D. | 水最终不可能充满整个烧瓶 |
16.下列关于苯的叙述中正确的是( )
| A. | 苯分子中碳碳键为单双键交替结构 | |
| B. | 苯中含有碳碳双键,所以苯属于烯烃 | |
| C. | 苯与氢气在一定条件下反应生成环己烷 | |
| D. | 苯可以与溴水反应而使其褪色 |
17.对于反应A2+3B2=2C来说,以下表示中,反应速率最快的是( )
| A. | v(B2)=0.8 mol/(L•s) | B. | v(A2)=0.5 mol/(L•s) | C. | v(C)=0.9 mol/(L•s) | D. | v(B2)=1.2 mol/(L•s) |
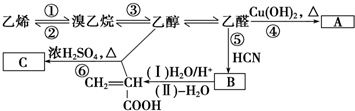
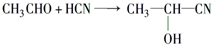 ;加成反应.
;加成反应.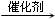
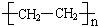 .
.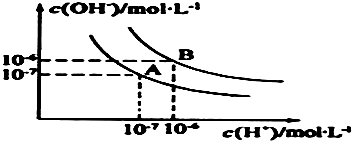 水的电离平衡曲线如图所示:
水的电离平衡曲线如图所示: