题目内容
 试运用所学知识,解决下列问题:
试运用所学知识,解决下列问题:(1)已知在一定温度下,
C(s)+CO2(g)?2CO(g) 平衡常数K1;
CO(g)+H2O(g)?H2(g)+CO2(g) 平衡常数K2;
C(s)+H2O(g)?CO(g)+H2(g) 平衡常数K3;
则K1、K2、K3之间的关系是:K3=
(2)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题.已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g)?H2(g)+CO2(g),该反应平衡常数随温度的变化如下表所示:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
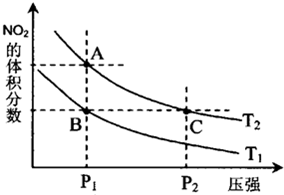
(3)从氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如NO、NO2、N2O4等.对反应N2O4(g)?2NO2(g)△H>0在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.B、C两点的气体的平均相对分子质量:B<C
D.由状态B到状态A,可以用加热的方法
(4)0.2mol/L的NaOH与0.4mol/L的硝酸铵溶液等体积混合后,溶液中各离子的物质的量浓度从大到小的顺序是
(5)工业上用CH3OH、氧气、KOH溶液构成燃料电池,则其负极电极反应式
考点:化学平衡常数的含义,常见化学电源的种类及其工作原理,化学平衡的影响因素,产物的百分含量随浓度、时间的变化曲线,化学平衡的计算
专题:基本概念与基本理论
分析:(1)根据平衡常数的表达式推断;
(2)温度升高K值减小,所以正反应为放热反应;令CO的浓度变化为c,用三段式表示出各物质变化的浓度、平衡时的浓度,再根据平衡常数计算;
(3)从平衡移动的角度分析各物理量的变化;
(4)首先让两者反应生成的物质考虑电离和水解,最终确定离子浓度的大小;
(5)在燃料电池的负极上是燃料发生失电子发生氧化反应,据此来书写;根据电极反应关系式求消耗气体的体积.
(2)温度升高K值减小,所以正反应为放热反应;令CO的浓度变化为c,用三段式表示出各物质变化的浓度、平衡时的浓度,再根据平衡常数计算;
(3)从平衡移动的角度分析各物理量的变化;
(4)首先让两者反应生成的物质考虑电离和水解,最终确定离子浓度的大小;
(5)在燃料电池的负极上是燃料发生失电子发生氧化反应,据此来书写;根据电极反应关系式求消耗气体的体积.
解答:
解:(1)根据化学方程式可知:K1=
,K2=
,K3=
,所以:K3=K1×K2,故答案为:K1×K2;
(2)温度升高K值减小,所以正反应为放热反应,
对于反应 CO(g)+H2O(g)?H2(g)+CO2(g),
开始(mol/L):0.02 0.02 0 0
变化(mol/L):c c c c
平衡(mol/L):0.02-c 0.02-c c c
所以
=9,解得c=0.015,
所以CO的转化率为
×100%=75%,
故答案为:放热;75%;
(3)对反应N2O4(g)?2NO2(g),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示.则
A.A点压强小于C点的压强,压强越大,反应速率越大,则反应速率:A<C,故A错误;
B.增大压强,平衡向正反应移动,但浓度的增大幅度大于转化的程度,所以C点浓度大,颜色深,故B错误;
C.B、C两点二氧化氮的体积分数相同,则混合气体的平均相对分子质量相同,故C错误;
D.在相同压强下,升高温度,平衡向逆反应方向移动,则二氧化氮的体积分数增大,所以由状态B到状态A,可以用加热的方法,故D正确;
故答案为:D;
(4)0.2mol/L的NaOH与0.4mol/L的硝酸铵溶液等体积混合后,得到等浓度的一水合氨、硝酸钠和硝酸铵的混合溶液,以一水合铵的电离为主,溶液呈碱性,所以c(NO3-)>c(NH4+)>c(Na+)>c(OH-)>c(H+),故答案为:c(NO3-)>c(NH4+)>c(Na+)>c(OH-)>c(H+);
(5)燃料电池中,负极上甲醇失电子发生氧化反应,电极反应式为:CH3OH-6e-+8OH-=CO32-+6H2O,正极反应的关系式为
O2 ~4mole-,
22.4L 4mole-
故答案为:CH3OH-6e-+8OH-=CO32-+6H2O;22.4;
| c2(CO) |
| c(CO2) |
| c(H2)×c(CO2) |
| c(CO)×c(H2O) |
| c(CO)×c(H2) |
| c(H2O) |
(2)温度升高K值减小,所以正反应为放热反应,
对于反应 CO(g)+H2O(g)?H2(g)+CO2(g),
开始(mol/L):0.02 0.02 0 0
变化(mol/L):c c c c
平衡(mol/L):0.02-c 0.02-c c c
所以
| c×c |
| (0.02-c)×(0.02-c) |
所以CO的转化率为
| 0.015mol/L |
| 0.02mol/L |
故答案为:放热;75%;
(3)对反应N2O4(g)?2NO2(g),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示.则
A.A点压强小于C点的压强,压强越大,反应速率越大,则反应速率:A<C,故A错误;
B.增大压强,平衡向正反应移动,但浓度的增大幅度大于转化的程度,所以C点浓度大,颜色深,故B错误;
C.B、C两点二氧化氮的体积分数相同,则混合气体的平均相对分子质量相同,故C错误;
D.在相同压强下,升高温度,平衡向逆反应方向移动,则二氧化氮的体积分数增大,所以由状态B到状态A,可以用加热的方法,故D正确;
故答案为:D;
(4)0.2mol/L的NaOH与0.4mol/L的硝酸铵溶液等体积混合后,得到等浓度的一水合氨、硝酸钠和硝酸铵的混合溶液,以一水合铵的电离为主,溶液呈碱性,所以c(NO3-)>c(NH4+)>c(Na+)>c(OH-)>c(H+),故答案为:c(NO3-)>c(NH4+)>c(Na+)>c(OH-)>c(H+);
(5)燃料电池中,负极上甲醇失电子发生氧化反应,电极反应式为:CH3OH-6e-+8OH-=CO32-+6H2O,正极反应的关系式为
O2 ~4mole-,
22.4L 4mole-
故答案为:CH3OH-6e-+8OH-=CO32-+6H2O;22.4;
点评:本题考查化学平衡常数、平衡移动相关计算、原电池等,题目较为综合,涉及多方面的知识,难度中等,本题中注意把握等效平衡的解题应用.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、将水杨酸、乙酸酐和浓硫酸在锥形瓶中混合后,85-90℃水浴加热5-10min,取出锥形瓶,置于冰水浴中,使阿司匹林结晶析出,为了使其结晶完全需要向锥形瓶中继续加适量的水 |
| B、用移液管取液后,将移液管稍倾斜放入锥形瓶中,并使管尖与容器内壁接触,松开食指使溶液全部流出,数秒后,取出移液管 |
| C、相同条件下,10mL 0.1mol/L FeCl2溶液中滴入1mL 0.1mol/L NaNO2溶液,溶液颜色由浅绿色变成黄色,10mL 0.1mol/L KI溶液中滴入1mL 0.1mol/L NaNO2溶液,溶液颜色无变化,说明溶液的pH会影响NO2-的氧化性 |
| D、为了检验火柴头中的硫元素,先用刀片削下几根火柴的火柴头,放入一支中号试管中,先用酒精灯加热该试管底部引燃“火药”,然后塞上橡皮塞待用 |
某反应过程能量变化如图所示,下列说法正确的是( )


| A、反应过程a有催化剂参与 |
| B、该反应为放热反应,热效应等于△H |
| C、改变催化剂,可改变该反应的活化能 |
| D、在催化剂条件下,反应的活化能等于E1+E2 |
下列化学用语表示正确的是( )
A、原子核中有6个中子的硼原子:
| ||
B、HCl的电子式: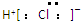 | ||
C、K+结构示意图: | ||
| D、HClO的结构式:H-O-Cl |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、0.1mol?L-1 Na2S溶液中含有的Na+离子数为0.2NA |
| B、50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA |
| C、标准状况下,22.4L以任意比例混合的氢气和氯气混合气中含有的原子总数为2NA |
| D、0.10mol Fe粉与足量水蒸气反应生成的H2分子数为0.10NA |




