题目内容
下列各组离子在指定溶液中,能大量共存的是
A.含有NaClO的溶液中:K+,NH4+, Fe3+,Br-,SO32-
B.所含溶质为Na2S2O3的溶液:K+、SO42-、NO3-、H+
C.加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,K+,SO42-
D.使甲基橙变红的溶液中:Fe2+,MnO4-,Na+,SO42-
C
【解析】
试题分析:A、次氯酸钠与亚硫酸根离子发生氧化还原反应,不能大量共存,错误;B、含有硝酸的溶液中Na2S2O3与硝酸发生氧化还原反应,生成硫酸根离子,不能大量共存,错误;C、与Mg反应放出氢气的溶液为酸性溶液,在酸性溶液中,四种离子都不反应,可以大量共存,正确;D、使甲基橙变红色的溶液为酸性溶液,酸性溶液中高锰酸根离子与亚铁离子发生氧化还原反应生成铁离子和锰离子,不能大量共存,错误,答案选C。
考点:考查给定条件的离子大量共存

(8分)某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL。试回答下列问题:
(1)锥形瓶中的溶液从 色变为 色时,停止滴定。
(2)滴定时边滴边摇动锥形瓶,眼睛应观察
A、滴定管内液面的变化
B、锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是 由此造成的测定结果 (偏高、偏低或无影响)
(4)步骤②缺少的操作是
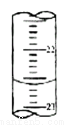
(5)下图,是某次滴定时的滴定管中的液面,其读数为 mL
(6)根据下列数据:
滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 25.00 | 0.50 | 20.40 |
第二次 | 25.00 | 4.00 | 24.10 |
请计算待测烧碱溶液的浓度(保留四位小数) mol/L


