题目内容
8.一定质量的碳和8g氧气在密闭容器中于高温下反应,恢复到原来的温度,测得容器内的压强变为原来的1.8倍,则参加反应的碳的质量为( )| A. | 3.0 g | B. | 5.4g | C. | 6 g | D. | 无法确定 |
分析 发生C+O2$\frac{\underline{\;高温\;}}{\;}$CO2、2C+O2$\frac{\underline{\;高温\;}}{\;}$2CO,由方程式可知只发生前者则压强与原来的相同,只发生后者则压强是原来的2倍;测得容器内的压强变为原来的1.8倍,说明上述两反应发生,即生成CO2和CO的混合物,以此来解答.
解答 解:n(O2)=$\frac{8g}{32g/mol}$=0.25mol,反应后容器内的压强变为原来的1.8倍,则CO2和CO的混合物的物质的量为0.25mol×1.8=0.45mol,由C原子守恒可知,参加反应的碳的质量为0.45mol×12g/mol=5.4g,
故选B.
点评 本题考查化学反应的计算,为高频考点,把握发生的反应、物质的量与压强的关系、原子守恒为解答的关键,侧重分析与计算能力的考查,注意守恒法的应用,题目难度不大.

练习册系列答案
相关题目
16.分别取等质量的两种烃完全燃烧,生成CO2及消耗O2的量均相同,这两种烃之间的关系正确的是( )
| A. | 只能是同种物质 | B. | 一定是同系物,有相同的通式 | ||
| C. | 实验式一定相同 | D. | 一定互为同分异构体 |
13.某元素原子的质量数为A,它的阳离子Xn+核外有x个电子,w克这种原子的原子核内中子的物质的量为( )
| A. | $\frac{w(A+x-n)}{A}$mol | B. | $\frac{A(A-x+n)}{w}$mol | C. | $\frac{w(A-x-n)}{A}$mol | D. | $\frac{w(A+x+n)}{A}$mol |
20.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 1.0mol•L-lKNO3溶液:H+、Fe2+、Cl-、SO42- | |
| B. | 与铝粉反应放出氢气的无色溶液中:NO3-、Mg2+,Na+、SO42- | |
| C. | 0.1 mol•L-1 FeCl3溶液:K+、NH4+、Cl-、S2- | |
| D. | 在无色透明溶液中:Ba2+、Ca2+、NO3-、Cl- |
17.下列变化中,属于物理变化的是( )
| A. | 从石油中分馏出汽油 | B. | 煤的气化制水煤气 | ||
| C. | 煤的干馏制焦炭 | D. | 油脂的水解制肥皂 |
20.只含镁、镍和碳三种元素的新型超导晶体的一个晶胞如图所示,则该晶体的化学式为( )
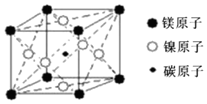

| A. | MgCNi3 | B. | MgC2Ni | C. | MgCNi2 | D. | Mg2CNi3 |
 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验