题目内容
16.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )| A. | 标准状况下,22.4L的CH3Cl中所含质子数为26NA | |
| B. | 将100mL0.1mol/L的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒的数目为0.01NA | |
| C. | 常温下,1L0.1mol/L醋酸中含有的离子总数为0.2NA | |
| D. | 0.1molC2H2气体中,原子间含有的共用电子对数目为0.3NA |
分析 A、求出一氯甲烷的物质的量,然后根据一氯甲烷中含26个质子来分析;
B、一个氢氧化铁胶粒是多个氢氧化铁的聚集体;
C、醋酸是弱电解质,不能完全电离;
D、在乙炔中含5对共用电子对.
解答 解:A、标况下22.4L一氯甲烷的物质的量为1mol,而一氯甲烷中含26个质子,故1mol一氯甲烷中含26NA个质子,故A正确;
B、一个氢氧化铁胶粒是多个氢氧化铁的聚集体,故形成的胶粒的个数小于0.01NA个,故B错误;
C、醋酸是弱电解质,不能完全电离,故溶液中的离子的个数小于0.2NA个,故C错误;
D、在乙炔中含5对共用电子对,故0.1mol乙炔气体中含有0.5NA对共用电子对,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
相关题目
6.新一代饮用水的消毒剂ClO2具有高效、广谱、安全等特点.制取ClO2的其中一种反应是:Cl2+2NaClO2═2ClO2+2NaCl.则下列叙述正确的是( )
| A. | 该反应是复分解反应 | B. | 该反应1molCl2得到2mole- | ||
| C. | 反应中Cl2既是氧化剂,又是还原剂 | D. | NaClO2和ClO2中Cl的化合价相同 |
7.分子组成为C6HmO3N3Cl的有机物分子中,m最大值为( )
| A. | 14 | B. | 16 | C. | 18 | D. | 20 |
4.利用反应:B(OCH3)3+4NaH=NaBH4+3CH3ONa制备NaBH4.下列说法不正确的是( )
| A. | NaBH4的电子式为 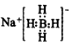 | |
| B. | 该反应在无水环境中进行 | |
| C. | NaBH4是很好的还原剂,常用于有机合成 | |
| D. | 1 molNaBH4与水充分反应可生成标况下44.8LH2 |
11.1914年报道的第一种常温离子液体硝酸乙基铵[(C2H5NH3)NO3],是通过HNO3与C2H5NH2反应制得,其熔点为12℃.下列有关硝酸乙基铵的说法正确的是( )
| A. | 常温下能导电 | B. | 水溶液呈碱性 | ||
| C. | 是共价化合物 | D. | 能与NaOH反应产生NH3 |
1.甲、乙、丙、X是中学化学中常见的4种物质,其转化关系如图,其中甲和X不可能是( )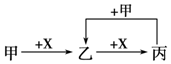

| A. | 甲为C2H5OH、X为O2 | B. | 甲为H2S、X为O2 | ||
| C. | 甲为HNO3、X为Fe | D. | 甲为AlCl3溶液、X为NaOH溶液 |
5.重水(${\;}_{1}^{2}$H2O)是重要的核工业原料,关于氘原子(${\;}_{1}^{2}$H)说法错误的是( )
| A. | 氘原子核外有1个电子 | B. | 氘原子质量数为2 | ||
| C. | 一个氘原子中含有2个中子 | D. | 与氕原子互为同位素 |
10.下列反应中,熵显著增加的是( )
| A. | CO(g)+2H2(g)=CH3OH(g) | |
| B. | CaCO3(g)+2HCl(aq)=CaCl2(aq)+H2O(l)+CO2(g) | |
| C. | C(s)+O2(g)=CO2(g) | |
| D. | 2Hg(l)+O2(g)=2HgO(s) |
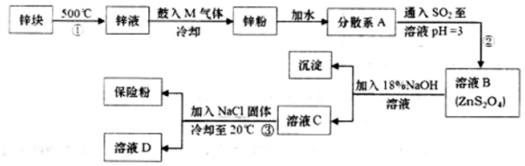
 ;悬浊液; (填“溶液”“胶体”或“悬浊液”).
;悬浊液; (填“溶液”“胶体”或“悬浊液”).