题目内容
16.配平方程式,:□KMnO4+□HCl-□KCl+□MnCl2+□Cl2↑+□H2O
上式反应中的氧化剂是KMnO4,还原产物是MnCl2被氧化的元素是Cl,每生成1molCl2转移的电子数目为2mol,氧化产物与还原产物的物质的量之比为5:2.
分析 反应中锰元素化合价变化为:+7→+2;部分氯元素化合价变化为:-1→0;依据氧化还原反应得失电子守恒结合原子个数守恒书写氧化还原反应方程式,依据反应中元素化合价变化判断氧化剂、还原产物,被氧化元素,依据方程式计算电子转移数目,氧化产物与还原产物的物质的量之比.
解答 解:反应中锰元素化合价变化为:+7→+2;部分氯元素化合价变化为:-1→0,要使得失电子守恒,则高锰酸钾系数为2,氯气系数为5,依据原子个数守恒,氯化锰系数为2,氯化钾系数为2,氯化氢系数为16,水系数为8,方程式:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,反应中锰元素化合价降低,所以高锰酸钾做氧化剂,对应产物氯化锰为还原产物;氯元素化合价升高,被氧化,氯气为氧化产物;生成1mol氯气转移2mol电子;氧化产物与还原产物的物质的量之比为:5:2;
故答案为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O;KMnO4;MnCl2;Cl;2mol;5:2.
点评 本题考查了氧化还原反应基本概念及电子转移数目计算,明确氧化还原反应得失电子守恒是解题关键,题目难度不大.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
6.肉制品加工中,使用护色剂--亚硝酸钠必须严格控制用量,确保食品安全.某一反应体系共有反应物和生成物六种物质:NaNO2、H2O、NO、I2、NaI、HI.已知该反应中NaNO2只发生了如下过程:NaNO2→NO.下列有关说法不正确的是( )
| A. | 氧化剂与还原剂的物质的量之比为1:2 | |
| B. | 若有1mol电子转移,则氧化产物的物质的量是0.5mol | |
| C. | 据此反应原理,可以在酸性条件下用淀粉碘化钾试纸检验NO${\;}_{2}^{-}$的存在 | |
| D. | 若误食亚硝酸钠会导致血红蛋白中亚铁离子转化为铁离子而中毒 |
7.设NA为阿伏加德罗常数,下列说法中正确的是( )
| A. | 10g 质量分数为46%的乙醇水溶液中所含氢原子数为0.6NA | |
| B. | 将标准状况下22.4LNO与11.2LO2混合后的体积约为22.4L | |
| C. | 在反应KClO4+8HCl═KCl+4Cl2↑+4H2O中,每生成4molCl2转移的电子数为7NA | |
| D. | 6g石英晶体中含有的Si-O键数为0.2NA |
11.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 在室温和常压下,71 g Cl2含有2NA个Cl原子 | |
| B. | 在同温、同压下,相同体积的任何气体,所含分子数和原子数都相同 | |
| C. | 物质的量浓度为1 mol/L的K2SO4溶液中,含2NA个K+ | |
| D. | 100g 98%的硫酸溶液中所含氢原子的数目为2NA |
1.一块表面已被氧化为Na2O的钠块10.8g,将其投入100g水中,产生H20.2g,则被氧化的钠是( )
| A. | 9.2g | B. | 10.6g | C. | 6.2g | D. | 4.6g |
8.某二元弱酸(H2A)溶液按下式发生一级电离和二级电离:H2AHA-+H+HA-A2-+H+下列溶液中C(A2-)最大的是( )
| A. | 0.01 mol•L-1的H2A溶液 | |
| B. | 0.01 mol•L-1NaHA溶液 | |
| C. | 0.02 mol•L-1HCl溶液与0.04 mol•L-1NaHA溶液等体积混合 | |
| D. | 0.02mol•L-1 NaOH溶液0.02 mol•L-1 NaHA溶液等体积混合 |
5.常温下,一定量冰醋酸加水稀释过程中,溶液的导电性如下图所示.下列说法正确的是( )
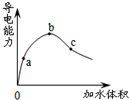

| A. | pH值:b>a>c | |
| B. | 与锌反应起始速率:a=b=c | |
| C. | 水电离的c(H+) c>a>b | |
| D. | 加入足量的NaHCO3固体,产生气体体积:a>b>c |