题目内容
用食用白醋(醋酸浓度约为1mol/L)进行下列实验,能证明醋酸为弱电解质的是( )
| A、白醋中滴入石蕊试液呈红色 |
| B、白醋加入豆浆中有沉淀产生 |
| C、蛋壳浸泡在白醋中有气体放出 |
| D、白醋中c(H+)=0.01 moL/L |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:只要能说明醋酸在水溶液里部分电离就能证明醋酸为弱电解质,据此分析解答.
解答:
解:A.白醋中滴入石蕊试液呈红色,说明白醋为酸,但不能说明醋酸部分电离,所以不能证明醋酸为弱电解质,故A错误;
B.白醋加入豆浆中产生沉淀,说明白醋是电解质,但不能说明醋酸在水溶液里部分电离,所以不能证明醋酸是弱电解质,故B错误;
C.蛋壳浸泡在白醋中有气体放出,说明醋酸的酸性大于碳酸,但不能说明醋酸部分电离,则不能证明醋酸是弱电解质,故C错误;
D.白醋中c(H+)=0.01 moL/L<1mol/L,则说明白醋部分电离,则证明醋酸是弱电解质,故D正确;
故选D.
B.白醋加入豆浆中产生沉淀,说明白醋是电解质,但不能说明醋酸在水溶液里部分电离,所以不能证明醋酸是弱电解质,故B错误;
C.蛋壳浸泡在白醋中有气体放出,说明醋酸的酸性大于碳酸,但不能说明醋酸部分电离,则不能证明醋酸是弱电解质,故C错误;
D.白醋中c(H+)=0.01 moL/L<1mol/L,则说明白醋部分电离,则证明醋酸是弱电解质,故D正确;
故选D.
点评:本题考查了电解质强弱判断,根据电离程度确定电解质强弱,不能根据物质的溶解性大小、溶液酸碱性判断电解质强弱,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
化学反应都伴随有能量变化.下列反应中不能由化学能转化为电能的是( )
| A、酸碱中和反应 |
| B、金属锌与硫酸铜溶液反应 |
| C、乙醇燃烧 |
| D、金属铜溶于氯化铁溶液 |
反应H2(g)+Br2(l)═2HBr(g)在25℃、101kPa下进行,已知生成2molHBr放出热量为72kJ,蒸发1mol Br2(l)需要吸收的能量为30kJ,其他相关数据如下表:则表中a为( )
| 1mol分子中的化学键断时需要吸收能量/kJ | H2(g) | Br2(g) | HBr(g) |
| 436 | a | 369 |
| A、404 | B、260 |
| C、230 | D、200 |
聚四氟乙烯(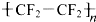 )是不粘锅涂覆物质的主要成分.下列关于聚四氟乙烯的说法,不正确的是( )
)是不粘锅涂覆物质的主要成分.下列关于聚四氟乙烯的说法,不正确的是( )
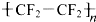 )是不粘锅涂覆物质的主要成分.下列关于聚四氟乙烯的说法,不正确的是( )
)是不粘锅涂覆物质的主要成分.下列关于聚四氟乙烯的说法,不正确的是( )| A、属于高分子化合物 |
| B、单体是CF2=CF2 |
| C、可由加聚反应得到 |
| D、能使高锰酸钾酸性溶液褪色 |
下列反应的离子方程式正确的是( )
| A、碳酸钙溶于盐酸:CO32-+2H+=H2O+CO2↑ |
| B、稀 H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ |
| C、KOH溶液与KHSO4溶液反应:OH-+H+=H2O |
| D、Ba(OH)2和(NH4)2SO4溶液混合加热:Ba2++SO42-=Ba SO4↓ |
在生活、生产中为增大反应速率而采取的措施合理的是( )
| A、塑料制品中添加抑制剂 |
| B、食物放在冰箱中 |
| C、燃煤发电时用煤粉代替煤块 |
| D、在糕点包装内放置小包除氧剂 |
下列比较正确的是( )
| A、化学键的键能由大到小:金刚石>碳化硅>硅>锗 |
| B、熔沸点由高到低:氯化钠>氧化铝>硅>二氧化碳 |
| C、硬度由大到小:C60>碳化硅>铁>氯化钠 |
| D、导电性能由强到弱:金>铜>石墨>二氧化碳 |
某有机物在氧气里充分燃烧,生成的CO2和H2O的物质的量之比为1:1,由此可以得出该有机物( )
| A、分子中C、H、O的个数比为1:2:3 |
| B、分子中C和H的个数比为1:2 |
| C、分子中肯定不一定含氧原子 |
| D、分子中肯定含有氧原子 |
下列说法正确的是( )
| A、500mL 2 mol/L葡萄糖溶液中所含分子数是6.02×1023 |
| B、0.1mol/L Na2CO3溶液中的阴离子总数大于0.1×6.02×1023 |
| C、电解精炼铜时,若阳极质量减少64g,则外电路导线上通过的电子数不一定是2×6.02×1023 |
| D、5.6g铁粉在0.1mol氯气中充分燃烧,转移电子数是0.3×6.02×1023 |