题目内容
将10.2克氧化铝溶于浓度为1.24mol?L-1 500mL的盐酸中,充分反应后,再逐滴加入1mol?L-1的氢氧化钠溶液,试回答:
(1)加入氢氧化钠溶液多少体积时开始出现沉淀?
(2)加入氢氧化钠溶液多少体积时沉淀量最大?
(3)加入氢氧化钠溶液多少体积时沉淀恰好完全消失?
(1)加入氢氧化钠溶液多少体积时开始出现沉淀?
(2)加入氢氧化钠溶液多少体积时沉淀量最大?
(3)加入氢氧化钠溶液多少体积时沉淀恰好完全消失?
考点:化学方程式的有关计算
专题:计算题
分析:(1)首先氧化铝与盐酸反应生成氯化铝,由方程式确定两者之间的关系,根据已知量,确定盐酸过量,加入氢氧化钠首先将过量的酸反应掉,然后氯化铝与氢氧化钠反应生成氢氧化铝沉淀;
(2)沉淀最大量时溶液是单一的氯化钠溶液,根据氯化钠的组成,得盐酸的物质的量与氢氧化钠的物质的量相等;
(3)沉淀恰好完全消失得到的是氯化钠和偏铝酸钠的混合溶液,根据物料守恒可知:n(NaOH)=2n(Al2O3)+n(HCl).
(2)沉淀最大量时溶液是单一的氯化钠溶液,根据氯化钠的组成,得盐酸的物质的量与氢氧化钠的物质的量相等;
(3)沉淀恰好完全消失得到的是氯化钠和偏铝酸钠的混合溶液,根据物料守恒可知:n(NaOH)=2n(Al2O3)+n(HCl).
解答:
解:(1)10.2g氧化铝为:
=0.1mol,500ml1.24mol?L-1 盐酸的物质的量为500ml×1.24mol?L-1×10-3L/ml=0.62mol,根据反应关系式
Al2O3+6HCl═2AlCl3+3H2O,溶解全部Al2O3需要0.6molHCl,所以盐酸过量,剩余盐酸的物质的量为:0.02mol,然后有AlCl3+3NaOH═Al(OH)3↓+3NaCl,所以,加入0.02molNaOH后开始有沉淀,所以加入氢氧化钠溶液体积为:
=0.02L,
答:加入氢氧化钠溶液0.02L时开始出现沉淀;
(2)沉淀最大量时溶液是单一的氯化钠溶液,根据氯化钠的组成,得盐酸的物质的量与氢氧化钠的物质的量相等,所以氢氧化钠的物质的量为:0.62mol,所以加入氢氧化钠溶液体积为:
=0.62L,
答:加入氢氧化钠溶液0.62L时沉淀量最大;
(3)沉淀恰好完全消失得到的是氯化钠和偏铝酸钠的混合溶液,根据物料守恒可知:n(NaOH)=2n(Al2O3)+n(HCl)=2×0.1mo+0.62mol=0.82mol,所以加入氢氧化钠溶液体积为:
=0.82L,
答:加入氢氧化钠溶液0.82L时沉淀恰好完全消失.
| 10.2g |
| 102g/mol |
Al2O3+6HCl═2AlCl3+3H2O,溶解全部Al2O3需要0.6molHCl,所以盐酸过量,剩余盐酸的物质的量为:0.02mol,然后有AlCl3+3NaOH═Al(OH)3↓+3NaCl,所以,加入0.02molNaOH后开始有沉淀,所以加入氢氧化钠溶液体积为:
| 0.02mol |
| 1mol?L-1 |
答:加入氢氧化钠溶液0.02L时开始出现沉淀;
(2)沉淀最大量时溶液是单一的氯化钠溶液,根据氯化钠的组成,得盐酸的物质的量与氢氧化钠的物质的量相等,所以氢氧化钠的物质的量为:0.62mol,所以加入氢氧化钠溶液体积为:
| 0.62mol |
| 1mol?L-1 |
答:加入氢氧化钠溶液0.62L时沉淀量最大;
(3)沉淀恰好完全消失得到的是氯化钠和偏铝酸钠的混合溶液,根据物料守恒可知:n(NaOH)=2n(Al2O3)+n(HCl)=2×0.1mo+0.62mol=0.82mol,所以加入氢氧化钠溶液体积为:
| 0.82mol |
| 1mol?L-1 |
答:加入氢氧化钠溶液0.82L时沉淀恰好完全消失.
点评:本题考查金属氧化物与酸及盐与碱反应,明确生成沉淀最大时钠与氯元素的存在形式是解答本题的关键,然后利用关系式法即可计算解答.

练习册系列答案
相关题目
短周期元素W、X、Y、Z的原子序数依次增大,其简单离子不能破坏水的电离平衡的是( )
| A、W- |
| B、X+ |
| C、Y3+ |
| D、Z2- |
青石棉是一种致癌物质,是《鹿特丹公约》中受限制的46种化学品之一,其化学式为Na2Fe5Si8O22(OH)2.青石棉用稀硝酸溶液处理时,还原产物只有NO,下列说法不正确的是( )
| A、青石棉是一种硅酸盐材料 |
| B、青石棉中含有一定量的石英晶体 |
| C、青石棉的化学组成可表示为Na2O?3FeO?Fe2O3?8SiO2?H2O |
| D、1 mol青石棉能将含1 mol HNO3的稀硝酸还原 |
下列化学用语书写正确的是( )
A、甲烷的电子式: |
B、丙烯的键线式: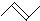 |
C、乙醚的结构式: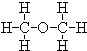 |
| D、乙烯的结构简式:CH2CH2 |
进行化学实验必须注意安全,下列说法不正确的是( )
| A、点燃氢气前要检验氢气的纯度,以免发生爆炸 |
| B、不慎将浓盐酸沾到皮肤上,要立即用浓碱溶液冲洗 |
| C、CO气体有毒,处理CO尾气时可将其点燃,转化为无毒的CO2 |
| D、如果少量酒精失火燃烧,可用湿抹布盖灭火焰 |
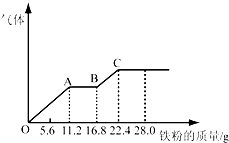 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示.下列分析或结果不正确的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示.下列分析或结果不正确的是( )| A、混合酸中HNO3物质的量浓度为2mol?L-1 |
| B、OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 |
| C、原混合酸中H2SO4物质的量为0.4 mol |
| D、第二份溶液中最终溶质为FeSO4 |