题目内容
向CuSO4饱和溶液中加入一块胆矾,一段时间后发现( )
| A、胆矾的形状和质量都没有改变 |
| B、胆矾的形状和质量都改变了 |
| C、胆矾的形状改变了,但质量没有变 |
| D、胆矾的质量减小了 |
考点:溶解度、饱和溶液的概念
专题:物质的量浓度和溶解度专题
分析:所谓的饱和溶液,指的是在一定温度下,一定剂量的溶剂里面,不能再继续溶解溶质的状态,此时达到了溶解和结晶的平衡状态,据此分析胆矾的质量有无变化.
解答:
解:因为溶液已经饱和,此时存在溶解和结晶的动态平衡,故不能再溶解硫酸铜,所以胆矾质量不变.,而溶解平衡是动态的平衡,故虽然胆矾的质量不变,但形状可以变,可由不规则变为规则.
A、胆矾的形状应该改变了,故A错误.
B、胆矾的质量没变,故B错误.
C、胆矾的形状改变了,但质量没有变,故C正确.
D、胆矾的质量不变,故D错误.
故选C.
A、胆矾的形状应该改变了,故A错误.
B、胆矾的质量没变,故B错误.
C、胆矾的形状改变了,但质量没有变,故C正确.
D、胆矾的质量不变,故D错误.
故选C.
点评:本题考查了饱和溶液中存在的溶解平衡,应注意一旦达到溶解平衡,即溶解和结晶的速率相同,此时加入溶质,溶质不能再溶解.

练习册系列答案
相关题目
下列有关原电池的叙述正确的是( )
| A、把电能转变为化学能,使溶液发生氧化还原反应 |
| B、电子从活泼金属流向不活泼金属,不活泼金属为负极 |
| C、外电路中电子从负极流向正极 |
| D、正极发生氧化反应 |
有机化合物A的分子式是C13H20O8(相对分子质量为304),1mol A在酸性条件下水解得到4mol CH3COOH和1mol B.B分子结构中每一个连有羟基的碳原子上还连有两个氢原子.B不能发生的反应是( )
| A、氧化反应 | B、取代反应 |
| C、消去反应 | D、加聚反应 |
亮菌甲素适用于治疗急性胆囊炎,其结构简式如图.下列有关叙述正确的是( )
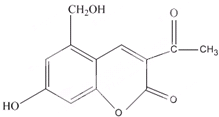

| A、亮菌甲素分子式为C12H11O5 |
| B、1mol亮菌甲素最多能与6mol H2发生加成反应 |
| C、1mol亮菌甲素与NaOH溶液反应,最多消耗3mol NaOH |
| D、亮菌甲素具有弱酸性体现了羟基对苯环的影响 |
下列离子方程式不正确的是( )
| A、向AgCl悬浊液中加入Na2S溶液:2AgCl+S2-═Ag2S+2Cl- |
| B、向NaHCO3溶液中加入NaOH溶液:HCO3-+OH-═CO2↑+H2O |
| C、向Ba(OH)2溶液中加入稀H2SO4:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| D、向Cu粉中加入过量的浓HNO3:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O |
在某100mL混酸中,硝酸的物质的量浓度为0.4mol?L-1,硫酸的物质的量浓度为0.2mol?L-1.向其中加入2.56g铜粉,微热,待充分反应后,溶液中Cu2+的物质的量浓度为( )
| A、0.15 mol?L-1 |
| B、0.3 mol?L-1 |
| C、0.225 mol?L-1 |
| D、无法计算 |
常温下,下列各组离子在指定的溶液中可能大量共存的是( )
| A、无色透明的溶液中:K+、NH4+、MnO4-、SO42- |
| B、含大量Fe3+的溶液中:Na+、Cu2+、NO3-、I- |
| C、乙醇溶液中:CH3COO-、Al3+、SO42-、Cl- |
| D、由水电离出的c(H+)=1.0×10-11?L-1的溶液中:Fe(OH)3胶体、Ba2+、OH-、Cl- |
某元素的最高价氧化物的分子式RO2其中含R 27.27%,对此元素的叙述不正确的是( )
| A、该元素为硫 |
| B、该元素的气态氢化物含H为25% |
| C、RO2分子中含极性键 |
| D、RO2与水反应能生成酸 |
总质量一定时,不论以任何比例混合,完全燃烧生成CO2与H2O的量为定值的是( )
A、 和C2H4 和C2H4 |
| B、C2H4和C3H8 |
| C、CH2O和C2H4O2 |
| D、C3H8O和C2H6O |