题目内容
14.下列说法正确的是( )| A. | 可根据硫酸密度的大小判断铅蓄电池是否需要充电 | |
| B. | 当物质中的化学键发生断裂时,一定发生化学变化 | |
| C. | 淀粉和纤维素的化学式均为(C6H10O5)n,故互为同分异构体 | |
| D. | 只由一种元素的阳离子与另一种元素的阴离子组成的物质一定是纯净物 |
分析 A、铅蓄电池充电反应为2PbSO4+2H2O=Pb+PbO2+2H2SO4,充电过程中生成硫酸,硫酸密度增大;
B、离子键在熔融状态下一定断裂,某些共价键在水溶液中可能断裂;
C、淀粉和纤维素的n的取值范围不同;
D、一种元素形成的阳离子可能有多种,一种元素形成的阴离子也可能有多种.
解答 解:A、铅蓄电池充电反应为2PbSO4+2H2O=Pb+PbO2+2H2SO4,充电过程中生成硫酸、消耗水,所以硫酸密度增大,则可根据硫酸密度的大小来判断铅蓄电池是否需要充电,故A正确;
B、离子键在熔融状态下一定断裂,如氯化钠在熔融状态下,离子键断裂,但不是化学变化;某些共价键在水溶液中可能断裂,如HCl气体溶于水后,共价键断裂,但也不是化学变化,故B错误;
C、淀粉和纤维素的n的取值范围不同,故淀粉和纤维素的分子式不同,则不是同分异构体,故C错误;
D、一种元素形成的阳离子可能有多种,如铁元素形成的阳离子可能为Fe3+,还可能为Fe2+,一种元素形成的阴离子也可能有多种,如氧元素形成的阴离子有O2-和O22-,故只由一种元素形成的阳离子与另一种元素的阴离子组成的物质不一定是纯净物,故D错误.
故选A.
点评 本题考查了化学反应的实质,为高频考点,涉及化学反应的实质、同分异构体的判断和纯净物混合物的判别等知识点,明确化学反应原理及物质结构的差异性是解本题关键,易错选项是D.

练习册系列答案
相关题目
4.光导纤维的主要化学成分( )
| A. | 二氧化硅 | B. | 硅 | C. | 硅酸 | D. | 硅酸钠 |
5.下列溶液中的c(Cl-)与50mL 1mol/L FeCl3溶液中的c(Cl-)相等的是( )
| A. | 150 mL 1 mol/L NaCl溶液 | B. | 75 mL 2 mol/L NH4Cl溶液 | ||
| C. | 75 mL 2 mol/L AlCl3溶液 | D. | 150 mL 1.5 mol/L MgCl2溶液 |
2.下列有关说法,不正确的是( )
①将盛有二氧化氮气体的试管倒立在水中,溶液会充满试管
②向煤中加入适量石灰石,在煤燃烧时最终生成CaSO4,可减少SO2对大气的污染
③为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化
④电解从海水中得到的氯化镁溶液可获得金属镁
⑤为证明NaHCO3溶液中混有Na2CO3,取少量溶液,加入澄清石灰水,若有白色沉淀生成,则证明混有Na2CO3
⑥用FeCl3溶液腐蚀铜制印刷电路板:2Fe3++Cu=2Fe2++Cu2+.
①将盛有二氧化氮气体的试管倒立在水中,溶液会充满试管
②向煤中加入适量石灰石,在煤燃烧时最终生成CaSO4,可减少SO2对大气的污染
③为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化
④电解从海水中得到的氯化镁溶液可获得金属镁
⑤为证明NaHCO3溶液中混有Na2CO3,取少量溶液,加入澄清石灰水,若有白色沉淀生成,则证明混有Na2CO3
⑥用FeCl3溶液腐蚀铜制印刷电路板:2Fe3++Cu=2Fe2++Cu2+.
| A. | 仅①③④⑤ | B. | 仅②③④ | C. | 仅①③④ | D. | 仅①②④⑤ |
9.原计划实现全球卫星通讯需发射77颗卫星,这与铱(Ir)元素的原子核外电子数恰好相等,因此称为“铱星计划”.已知铱的一种同位素是19177Ir,则其核内的中子数与质子数之差是( )
| A. | 77 | B. | 37 | C. | 191 | D. | 114 |
19.下列分子只表示一种物质的是( )
| A. | C3H7Cl | B. | C3H8 | C. | C3H6 | D. | C |
6.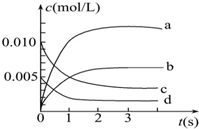 在2L密闭容器内,800℃时发生反应:2NO(g)+O2(g)═2NO2(g),在体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时发生反应:2NO(g)+O2(g)═2NO2(g),在体系中,n(NO)随时间的变化如表:
(1)上述反应是(填“是”或“不是”)可逆反应,在第5s时,NO的转化率为65%.
(2)如图中表示NO2变化曲线的是b.用O2表示从0~2s内该反应的平均速率v=0.001 5 mol/(L•s).
(3)能说明该反应已达到平衡状态的是bc.
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内气体密度保持不变.
 在2L密闭容器内,800℃时发生反应:2NO(g)+O2(g)═2NO2(g),在体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时发生反应:2NO(g)+O2(g)═2NO2(g),在体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| NO的物质的量(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)如图中表示NO2变化曲线的是b.用O2表示从0~2s内该反应的平均速率v=0.001 5 mol/(L•s).
(3)能说明该反应已达到平衡状态的是bc.
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内气体密度保持不变.
3.下列关于卤代烃的说法正确的是( )
| A. | 在卤代烃中,卤素原子与碳原子间形成共价键 | |
| B. | 在溴乙烷(CH3CH2Br)分子中,溴元素的存在形式为溴离子 | |
| C. | 聚四氟乙烯(塑料王)为高分子化合物,不属于卤代烃 | |
| D. | 卤代烃的沸点比相应烷烃的沸点低 |
4.已知有如下反应:
①2BrO3-+Cl2═Br2+2ClO3-
②ClO3-+5Cl-+6H+═3Cl2+3H2O
③2FeCl2+Cl2═2FeCl3
④2FeCl3+2KI═2FeCl2+2KCl+I2
下列各微粒氧化能力由强到弱的顺序正确的是( )
①2BrO3-+Cl2═Br2+2ClO3-
②ClO3-+5Cl-+6H+═3Cl2+3H2O
③2FeCl2+Cl2═2FeCl3
④2FeCl3+2KI═2FeCl2+2KCl+I2
下列各微粒氧化能力由强到弱的顺序正确的是( )
| A. | ClO3->BrO3->Cl2>Fe3+>I2 | B. | BrO3->Cl2>ClO3->I2>Fe3+ | ||
| C. | BrO3->ClO3->Cl2>Fe3+>I2 | D. | BrO3->ClO3->Fe3+>Cl2>I2 |