题目内容
10.下列表示对应化学反应的离子方程式正确的是( )| A. | 用氨水溶解氯化银沉淀:Ag++2NH3•H2O═[Ag(NH3)2]++2H2O | |
| B. | MgCO3与NaOH溶液反应生成沉淀:MgCO3+2OH-═Mg(OH)2↓+CO32- | |
| C. | 将NaHSO4与Ba(OH)2溶液混合至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| D. | 向NH4HSO4溶液中滴加过量NaOH溶液:NH4++HSO4-+2OH-═SO42-+NH3•H2O |
分析 A.氯化银为沉淀,应保留化学式;
B.氢氧化镁溶解度小于碳酸镁,碳酸镁可以转化为氢氧化镁沉淀;
C.将NaHSO4与Ba(OH)2溶液混合至中性反应生成硫酸钠、硫酸钡和水;
D.硫酸氢根离子为多元强酸的酸式根离子,应拆成离子形式.
解答 解:A.用氨水溶解氯化银沉淀,氯化银不能拆开,离子方程式为:AgCl+2NH3•H2O=[Ag(NH3)2]++2H2O+Cl-,故A错误;
B.MgCO3与NaOH溶液反应生成沉淀,离子方程式:MgCO3+2OH-═Mg(OH)2↓+CO32-,故B正确;
C.将NaHSO4与Ba(OH)2溶液混合至中性,离子方程式:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故C错误;
D.向NH4HSO4溶液中滴加过量NaOH溶液,离子方程式:NH4++H++2OH-═NH3•H2O+H2O,故D错误;
故选:B.
点评 本题考查了离子方程式的书写判断,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法,题目难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
1.在一定温度下,可逆反应A(g)+3B(g)?2C(g)达到平衡的标志是( )
| A. | A的生成速率与C分解的速率相等 | |
| B. | 单位时间生成nmolA,同时生成3nmolB | |
| C. | 单位时间生成nmolA,同时生成2nmolC | |
| D. | 单位时间生成B的速率与生成C的速率相等 |
18.下列离子方程式书写正确的是( )
| A. | 钠加入水中:Na+2H2O═Na++2OH-+H2↑ | |
| B. | Al2(SO4)3溶液中加入过量Ba(OH)2溶液:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| C. | Cl2通入水中 Cl2+H2O?2H++ClO-+Cl- | |
| D. | 向浓盐酸中加二氧化锰:MnO2+4H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$ Mn2++2H2O+Cl2↑ |
5.化学与STSE(社会、科学、技术和环境)密切相关,下列说法正确的是( )
①寻找合适催化剂提高合成氨工业中原料的转化率
②氟氯烃因能降低臭氧分解的活化能而加速臭氧的分解反应
③氟化物防止龋齿所涉及到的化学原理其实就是沉淀的转化
④煤气中毒或救治与氧气、一氧化碳和血红蛋白结合过程中的化学平衡移动有关.
①寻找合适催化剂提高合成氨工业中原料的转化率
②氟氯烃因能降低臭氧分解的活化能而加速臭氧的分解反应
③氟化物防止龋齿所涉及到的化学原理其实就是沉淀的转化
④煤气中毒或救治与氧气、一氧化碳和血红蛋白结合过程中的化学平衡移动有关.
| A. | ①②③ | B. | ②③④ | C. | ①④ | D. | ③④ |
15.金属锰主要用于高级合金的添加剂.以高铁菱锰矿(主要含MnCO3、FeCO3以及钴、镍等碳酸盐杂质、SiO2等)为原料制取金属锰的工艺流程如下:

下表列出了部分化合物的溶度积常数
(1)写出MnCO3溶浸时反应的化学方程式MnCO3+H2SO4=MnSO4+CO2↑+H2O.滤渣Ⅰ的主要成分为SiO2(填化学式).
(2)写出氧化时反应的离子方程式MnO2+4H+2Fe2+=Mn2++2Fe3++2H2O.
(3)加氨水调节溶液的pH至5.0~6.0,滤渣Ⅱ的主要成分为Fe(OH)3(填化学式),若溶液的pH偏高,将会导致溶液中锰元素的含量降低.
(4)若除杂后,溶液中Co2+、Ni2+的浓度均为1.0×10-5 mol•L-1,则c(S2-)最大=10-17mol•L-1.
(5)电解时阴极电极反应式为Mn2++2e-=Mn.

下表列出了部分化合物的溶度积常数
| 物质 | Fe(OH)3 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp | 4.0×10-38 | 2.0×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
(2)写出氧化时反应的离子方程式MnO2+4H+2Fe2+=Mn2++2Fe3++2H2O.
(3)加氨水调节溶液的pH至5.0~6.0,滤渣Ⅱ的主要成分为Fe(OH)3(填化学式),若溶液的pH偏高,将会导致溶液中锰元素的含量降低.
(4)若除杂后,溶液中Co2+、Ni2+的浓度均为1.0×10-5 mol•L-1,则c(S2-)最大=10-17mol•L-1.
(5)电解时阴极电极反应式为Mn2++2e-=Mn.
2.下列离子组在指定的溶液中能大量共存的是( )
| A. | 与铝粉反应放出H2的无色溶液:NO3-、Al3+、Na+、SO42- | |
| B. | 使红色石蕊试纸变蓝的溶液:SO42-、HCO3-、K+、Na+ | |
| C. | 中性溶液:Fe3+、Al3+、NO3-、SO42- | |
| D. | 常温下$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液:K+、AlO2-、CO32-、Na+、 |
20.美国科学家找到了一种突破目前锂离子电池充电量和充电速度限制的方法,该方法将硅簇置入石墨烯层之间,达到提升电池内部锂离子密度的效果,这种材料制成的新型锂电池充电容量和效率都比普通锂电池提高近十倍,下列有关说法正确的是( )
| A. | 电池工作时,锂电极为阳极,发生还原反应 | |
| B. | 电池充电时,Li+向阴极移动 | |
| C. | 该电池的化学能可完全转化为电能 | |
| D. | 新材料就是碳和硅化合而成的碳化硅材料 |
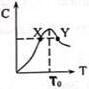 将物质的量均为3.00mol物质A、B混合于L容器中,发生如下反应3A+B?2C,再反应过程中C的物质的量分数随温度变化如图所示:
将物质的量均为3.00mol物质A、B混合于L容器中,发生如下反应3A+B?2C,再反应过程中C的物质的量分数随温度变化如图所示: