题目内容
5.下列实验装置能达到相应目的是( )| A. | 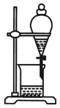 分离甘油和水 | B. | 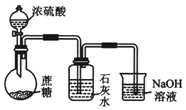 检验蔗糖与浓硫酸反应产生的CO2 | ||
| C. | 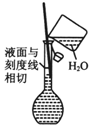 配制溶液 | D. | 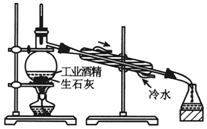 用工业酒精制取无水酒精 |
分析 A.甘油与水混溶;
B.二氧化硫、二氧化碳都石灰水反应生成沉淀;
C.应用胶头滴管定容;
D.酒精易挥发,可用蒸馏的方法分离.
解答 解:A.甘油与水混溶,溶液不分层,不能用分液的方法分离,故A错误;
B.浓硫酸与蔗糖反应,生成二氧化硫、二氧化碳等气体,二者都石灰水反应生成沉淀,不能检验是否生成二氧化碳,故B错误;
C.配制溶液定容时,应用胶头滴管,直接用玻璃棒引流易导致操作失败,故C错误;
D.生石灰可吸收谁,增大沸点差,可用蒸馏的方法分离,故D正确.
故选D.
点评 本题考查化学实验方案的评价,为高频考点,题目涉及物质的分离、检验以及溶液的配制等操作,侧重分析与实验能力的考查,注意实验的评价性和可行性的分析,题目难度不大.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
2.在实验室中,下列除去杂质的方法不正确的是( )
| A. | 硝基苯中混有浓硝酸,加入足量稀NaOH溶液洗涤,振荡,用分液漏斗分液 | |
| B. | 乙烯中混有SO2、CO2,将其通入NaOH溶液洗气 | |
| C. | 除去CO2中少量的SO2:气体通过盛饱和碳酸氢钠溶液的洗气瓶 | |
| D. | 乙烷中混有乙烯,通入氢气在一定条件下反应,使乙烯转化为乙烷 |
13.关于实验,下列正误判断、解释均正确的是( )


| 选项 | 实验目的 | 解释 | |
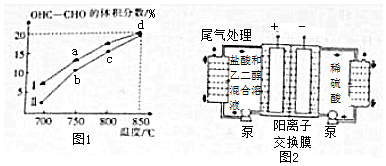
| A | 图1 | 检验产物 | 错误,乙醇也能使高锰酸钾褪色 |
| B | 图2 | 配制银氨溶液 | 错误,只能制得沉淀 |
| C | 图3 | 比较醋酸、碳酸、苯酚酸性强弱 | 正确,可以发生预期现象 |
| D | 图4 | 制取乙酸乙酯并分离 | 正确,用氢氧化钠可以除去乙酸 |
| A. | A | B. | B | C. | C | D. | D |
20.用下列实验装置进行相应实验,能达到实验目的是( )

| A. | 用图甲所示装置提纯氢氧化铁胶粒 | |
| B. | 用图乙所示装置进行中和热的测定 | |
| C. | 用图丙所示装置验证温度对平衡移动的影响 | |
| D. | 用图丙所示装置除去乙醇中的乙醚 |
10.下列叙述中正确的是( )
| A. | 由乙酸和乙醇生成乙酸乙酯的反应类型和由乙醇生成乙烯的反应类型相同 | |
| B. | 丙烯在一定条件下可与氯气发生取代反应生成3-氯丙烯 | |
| C. | 硫酸铵和硝酸铅均能使蛋白质变性 | |
| D. | 甲苯与氯气在光照下发生取代反应主要生成2,4-二氯甲苯 |
17.化学与生产、生活密切相关,下列有关说法正确的是( )
| A. | 轮船的船体外侧镶嵌一定量的锌块,可以减缓轮船被腐蚀的速度,称之为牺牲阳极的阴极保护法 | |
| B. | 工业生产中,常将氯气通入澄清石灰水中,制取漂白粉 | |
| C. | 氢氧燃料电池、铅蓄电池、硅太阳能电池都利用了原电池原理 | |
| D. | 夏天雷雨过后空气特别清新是因为空气中产生了少量二氧化氮 |
14.温度容积相同的3个密闭容器中,按不同方式投入反应物并保持恒温恒容,测得反应达到平衡时的有关数据如下(已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1 )
下列说法正确的是( )
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol N2、3molH2 | 2mol NH3 | 4mol NH3 |
| NH3的浓度(mol•L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | a1 | a2 | a3 |
| A. | 2 c1>c3 | B. | a1+a3<1 | C. | 2 p2<p1 | D. | a=b |
15.下列由实验得出的结论正确的是( )
| 实验 | 结论 | |
| A. | 将乙烯通入溴的四氯化碳溶液,溶液最终变为无色透明 | 生成的1,2-二溴乙烷无色、可溶于四氯化碳 |
| B. | 乙醇和水都可与金属钠反应产生可燃性气体 | 乙醇分子中的氢与水分子中的氢具有相同的活性 |
| C. | 用乙酸浸泡水壶中的水垢,可将其清除 | 乙酸的酸性小于碳酸的酸性 |
| D. | 甲烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红 | 生成的氯甲烷具有酸性 |
| A. | A | B. | B | C. | C | D. | D |